题目内容
【题目】下列离子方程式,书写正确的是( )
A.盐酸与石灰石反应:CO32ˉ+2H+ = CO2↑+H2O
B.铁与稀盐酸反应:2Fe+6H+ = 2Fe3++3H2↑
C.氢氧化铁胶体的制备:FeCl3 + 3H2O = Fe(OH)3+3HCl
D.硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42ˉ = BaSO4↓+Cu(OH)2↓
【答案】D
【解析】
A. 盐酸与石灰石反应生成氯化钙、二氧化碳和水,其中石灰石难溶于水,故离子方程式为:CaCO3+2H+ = CO2↑+H2O+Ca2+,故A错误;
B. 铁与稀盐酸反应生成氯化亚铁和氢气,离子方程式为:Fe+2H+ = Fe2++H2↑,故B错误;
C. 氢氧化铁胶体的制备的离子方程式为:Fe3++ 3H2O ![]() Fe(OH)3(胶体)+3HCl,故C错误;
Fe(OH)3(胶体)+3HCl,故C错误;
D. 硫酸铜溶液中滴加氢氧化钡溶液生成硫酸钡沉淀和氢氧化铜沉淀,离子方程式为:Ba2++2OH-+Cu2++SO42ˉ = BaSO4↓+Cu(OH)2↓,故D正确;
故选D。

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。

部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀 | 2.7 | 7.5 | 4.4 |
完全沉淀 | 3.7 | 9.7 | 6.7 |
请回答:
(1)溶液B中含有的阳离子有____________________(填离子符号)。
(2)下列物质中最适宜做氧化剂X的是__________(填字母)。
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,要调整pH范围是_____________,则试剂①可以选择______________(填化学式)。
(4)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是____________________________________(用离子方程式表示)。
(5)溶液E经过操作①可得到胆矾,操作①为________________________、过滤、洗涤。
(6)已知溶液中c(Cu2+)与pH的关系为lgc(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1mol/L,此时溶液中的Fe3+能否沉淀完全:___________(填“能”或“否”) 。
【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )
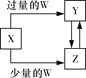
选项 | W | X |
A | 稀硫酸 | NaAlO2溶液 |
B | 稀硝酸 | Fe |
C | CO2 | Ca(OH)2溶液 |
D | Cl2 | Fe |
A. A B. B C. C D. D