题目内容
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。
请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是___。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②以物质的量之比为1:2在溶液中反应的离子方程式为___。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,还原产物是___(填名称)。
【答案】④⑥⑨ ①②③⑦⑨⑩ ⑤⑧ ![]()
![]() 二氧化氮
二氧化氮
【解析】
含有自由移动的电子或自由移动的离子可以导电,溶于水或在熔融状态下能够导电的化合物是电解质,溶于水和在熔融状态下均不能导电的化合物是非电解质。
①氢氧化钡固体中不存在自由移动的离子,不导电,可以在水中电离,属于电解质;
②KHSO4中不存在自由移动的离子,不导电,可以在水中电离,属于电解质;
③HNO3中不存在自由移动的离子,不导电,可以在水中电离,属于电解质;
④稀硫酸中存在自由移动的电子,导电,属于混合物,不属于电解质也不属于非电解质;
⑤二氧化碳气体中不存在自由移动的离子,不导电,不能电离,属于非电解质;
⑥铜是金属单质,可以导电,不属于电解质也不属于非电解质;
⑦碳酸钠粉末中不存在自由移动的离子,不导电,可以在水中电离,属于电解质;
⑧蔗糖晶体中不存在自由移动的离子,不导电,不能电离,属于非电解质;
⑨熔融氯化钠中存在自由移动的电子,导电,可以在水中电离,属于电解质;
⑩CuSO4·5H2O晶体中不存在自由移动的离子,不导电,可以电离,属于电解质;
(1)根据以上分析可知上述状态下可导电的是④⑥⑨,
故答案为:④⑥⑨;
(2)属于电解质的是①②③⑦⑨⑩,
故答案为:①②③⑦⑨⑩;
(3)属于非电解质的是⑤⑧,
故答案为:⑤⑧。
(4)硫酸氢钾是强酸的酸式盐,在水溶液中的电离方程式为![]() ,①与②在溶液中反应使溶液呈中性时生成硫酸钡、硫酸钾和水,反应的离子方程式为
,①与②在溶液中反应使溶液呈中性时生成硫酸钡、硫酸钾和水,反应的离子方程式为![]() ,
,
故答案为:![]() ;
;![]() ;
;
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O氮元素化合价降低,被还原,还原产物为NO2,名称为二氧化氮,
故答案为:二氧化氮。

 优加精卷系列答案
优加精卷系列答案【题目】(一)某实验小组利用如下装置(部分固定装置略)进行氮气与钙的反应,并探究其产物的性质及化学式。请回答下列问题。
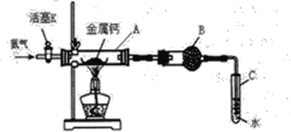
(1)反应过程中末端导管必须插入试管C的水中,目的是____。(填字母)
A.吸收反应中剩余的氮气
B.控制通入气体的流速
C.防止空气中的氧气倒流进入反应装置,干扰反应
(2)该小组同学认为根据相应的质量关系可以求出生成物的化学式,数据记录如下:
A的质量m0/g | A与钙的质量m1/g | A与产物的质量m2/g |
14.80 | 15.08 | 15.15 |
①通过计算得到化学式CaxN2,其中x=____。
②小组同学查阅资料得知产物为Ca3N2,能与水强烈反应,请写出Ca3N2与水反应的化学方程式_____。
(二)铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2![]() 6SO2+Fe3O4,若有3molFeS2参加反应,转移电子的物质的量为_____。
6SO2+Fe3O4,若有3molFeS2参加反应,转移电子的物质的量为_____。
(2)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为____。
(3)将一定量的Fe2O3溶于160mL 5molL-1盐酸中,再加入一定量铁粉,铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为____。