题目内容
15.由短周期元素形成的化合物有许多组成情况如果化学式为XY2,下列叙述正确的( )| A. | 如果XY2是共价化合物,则X与Y的原子序数不可能相差1 | |
| B. | 如果X与Y的原子序数相差6,则共价化合物XY2可溶于强碱溶液 | |
| C. | 如果X与Y的原子序数相差5,则离子化合物XY2不溶于水 | |
| D. | 如果XY2是离子化合物,则X与Y的原子序数可能相差9 |
分析 X、Y都是短周期元素,它们可能形成的化合物为XY2,X表现正化合价、Y表现负化合价,若为同周期,则原子序数Y>X,同周期从左到右原子半径逐渐减小,可能为CO2、NO2等;若X可以处于ⅡA、ⅣA族,Y为ⅥA、ⅤⅡA等,共价化合物如SiO2、CS2、BeCl2,离子化合物MgCl2等,以此来解答.
解答 解:A.XY2是共价化合物,则X与Y的原子序数可能相差1,如NO2,X为N,Y为O,故A错误;
B.如果X与Y的原子序数相差6,则共价化合物XY2可溶于强碱溶液,如SiO2,与强碱反应生成盐和水,故B正确;
C.如果X与Y的原子序数相差5,则离子化合物XY2可为MgCl2,溶于水,故C错误;
D.XY2是离子化合物,若为MgF2、MgCl2,则X与Y的原子序数之差均不大于5,故D错误;
故选B.
点评 本题考查了元素周期表的结构及应用,为高频考点,侧重于学生的分析能力的考查,把握周期表的结构及元素的位置、原子序数的关系等为解答的关键,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
10.下列实验能成功的是( )
| A. | 将乙酸和乙醇混合加热制乙酸乙酯 | |
| B. | 乙醇、浓硫酸加热到140℃制乙烯 | |
| C. | CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 | |
| D. | 用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀 |
20.已知下列热化学反应方程式( )
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8 kJ/mol
②Fe2O3(s)+$\frac{1}{3}$CO(g)=$\frac{2}{3}$Fe3O4(s)+$\frac{1}{3}$CO2(g)△H=-15.73 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.4 kJ/mol
则1molCO气体还原足量FeO固体得到Fe固体和CO2气体时对应的△H约为( )
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8 kJ/mol
②Fe2O3(s)+$\frac{1}{3}$CO(g)=$\frac{2}{3}$Fe3O4(s)+$\frac{1}{3}$CO2(g)△H=-15.73 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.4 kJ/mol
则1molCO气体还原足量FeO固体得到Fe固体和CO2气体时对应的△H约为( )
| A. | -218 kJ/mol | B. | -109 kJ/mol | C. | +218 kJ/mol | D. | +109 kJ/mol |
4.实验室配制一定物质的量浓度溶液时,下列仪器必不可少的是( )
| A. | 容量瓶 | B. | 试管 | C. | 烧瓶 | D. | 量筒 |
5.下列各物质的晶体中,晶体类型相同的是( )
| A. | CCl4 和NaCl | B. | I2和NaI | C. | SiO2和O2 | D. | CO2和H2O |

 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O.
+H2O. +2Na2CO3→
+2Na2CO3→ +2NaHCO3.
+2NaHCO3. .
.

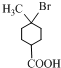 .
. ,
, .
. ,分子构型三角锥形.用电离方程式表示其水溶液呈碱性的原因NH3+H2O
,分子构型三角锥形.用电离方程式表示其水溶液呈碱性的原因NH3+H2O NH3•H2O
NH3•H2O