题目内容
7.氮的最常见的气态氢化物的名称为氨气,其电子式为 ,分子构型三角锥形.用电离方程式表示其水溶液呈碱性的原因NH3+H2O
,分子构型三角锥形.用电离方程式表示其水溶液呈碱性的原因NH3+H2O NH3•H2O
NH3•H2O  NH4++OH-.
NH4++OH-.
分析 氨气是无色、有刺激性气味的气体,氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对;氨气分子是三角锥形;氨气与水反应生成一水合氨,一水合氨为弱电解质,部分电离生成氢氧根离子,溶液显碱性,据此解答.
解答 解:氨气是氮的最常见的气态氢化物,为共价化合物,氮原子与三个氢原子分别共用1对电子,电子式为: ,分子为三角锥形结构,氨气与水反应生成一水合氨,一水合氨为弱电解质,部分电离生成氢氧根离子,溶液显碱性,电离方程式:NH3+H2O
,分子为三角锥形结构,氨气与水反应生成一水合氨,一水合氨为弱电解质,部分电离生成氢氧根离子,溶液显碱性,电离方程式:NH3+H2O  NH3•H2O
NH3•H2O  NH4++OH-;
NH4++OH-;
故答案为:氨气; ;三角锥形;NH3+H2O
;三角锥形;NH3+H2O  NH3•H2O
NH3•H2O  NH4++OH-;
NH4++OH-;
点评 本题考查了氨气的结构及性质,侧重考查学生对基础知识的掌握,题目难度不大,注意对基础知识的积累.

练习册系列答案
相关题目
17.有机化合物没食子茶素(EGC)结构简式如图所示.下列关于EGC的叙述中正确的是( )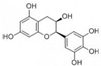

| A. | 分子中所有的原子共面 | |
| B. | 1mol EGC与4mol NaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,一定条件下可发生加成反应 | |
| D. | 易发生水解反应和显色反应,一定条件下可发生消去反应 |
18.砷(As)与其化合物常被运用在农药、除草剂、杀虫剂中.已知它与氮同主族,而与钙同周期,下列关于砷的有关描述中正确的是( )
| A. | 原子序数为23 | |
| B. | 最高价氧化物为As2O3,为酸性氧化物 | |
| C. | 原子半径比钙小 | |
| D. | 气态氢化物分子式为AsH3,稳定性强于NH3 |
15.由短周期元素形成的化合物有许多组成情况如果化学式为XY2,下列叙述正确的( )
| A. | 如果XY2是共价化合物,则X与Y的原子序数不可能相差1 | |
| B. | 如果X与Y的原子序数相差6,则共价化合物XY2可溶于强碱溶液 | |
| C. | 如果X与Y的原子序数相差5,则离子化合物XY2不溶于水 | |
| D. | 如果XY2是离子化合物,则X与Y的原子序数可能相差9 |
2.下列有关概念或原理的叙述正确的是 ( )
| A. | 氨基酸、蛋白质和氧化铝一样既能与酸反应,又能与碱反应,所以它们都是两性氧化物 | |
| B. | 制造婴儿用的一次性纸尿片采用的吸水保水的材料可以是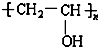 | |
| C. | 乙烯和聚乙烯都能使酸性KMnO4溶液褪色 | |
| D. | 甲酸乙酯、葡萄糖、麦芽糖、淀粉这四种物质的共同性质是,它们既可以发生水解反应,又可以发生银镜反应 |
12.下列化学用语的书写,正确的是( )
| A. | 氯原子的结构示意图: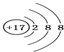 | |
| B. | 6个质子8个中子的碳元素的核素符号:12C | |
| C. | 氯化镁的电子式: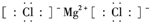 | |
| D. | 用电子式表示氯化氢的形成过程: |
 ;取代反应;.
;取代反应;.