题目内容
18.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )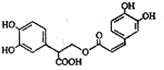
| A. | 迷迭香酸的分子式为C18H15O8 | |
| B. | 迷迭香酸可以发生加成、取代、显色反应 | |
| C. | lmol迷迭香酸跟H2反应,最多消耗6mol H2 | |
| D. | lmol迷迭香酸在NaOH溶液中反应,最多消耗5mol NaOH |
分析 该物质中含有苯环、酚羟基、羧基、酯基、碳碳双键,具有苯、酚、羧酸、酯、烯烃性质,能发生加成反应、加聚反应、氧化反应、还原反应、取代反应、水解反应等,据此分析解答.
解答 解:A.该物质分子式为C18H16O8,故A错误;
B.该物质中含有苯环、酚羟基、羧基、酯基、碳碳双键,具有苯、酚、羧酸、酯、烯烃性质,能发生加成反应、加聚反应、氧化反应、还原反应、取代反应、水解反应、显色反应等,故B正确;
C.苯环和碳碳双键能和氢气发生加成反应,所以lmol迷迭香酸跟H2反应,最多消耗7mol H2,故C错误;
D.酚羟基、酯基水解生成的羧基、羧基能和NaOH反应,所以lmol迷迭香酸在NaOH溶液中反应,最多消耗6mol NaOH,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,侧重考查酚、酯、烯烃等性质,易错选项是D.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.常温下,下列各组物质因存在氧化还原反应而不能共存的是( )
| A. | H+,C6H5O-,CH3COO-,MnO4- | B. | 葡萄糖,Cu2+,Na+,OH- | ||
| C. | Fe3+,NO3-,SO42-,H+ | D. | OH-,Al3+,NH4+,AlO2- |
15.将等物质的量的X、Y气体充入固定容积的密闭容器中,在一定条件下,发生如下反应并达到平衡:X(g)+Y(g)?2Z(g)△H<0.当改变某个条件建立新的平衡时,下表中关于新平衡与原平衡的比较正确的是 ( )
| 改变的条件 | 新平衡与原平衡比较 | |
| A | 向容器中充入He气 | X的转化率变大 |
| B | 增大压强 | X的浓度变大 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 使用适当催化剂 | X的体积分数变大 |
| A. | A | B. | B | C. | C | D. | D |
13.国际化学年的主题是“化学--我们的生活,我们的未来”.下列做法不正确的是( )
| A. | 利用露天焚烧方法处理塑料废弃物 | |
| B. | 利用高纯单质硅制成太阳能电池 | |
| C. | 利用微生物发酵技术,将植物秸秆、动物粪便等制成沼气 | |
| D. | 利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯塑料 |
3.(1)在1200℃时,天然气脱硫工艺中会发生下列反应:
①H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)═S(g)+H2O(g)△H3
④2S(g)═S2(g)△H4
则△H4的正确表达式为$\frac{2}{3}$(△H1+△H2-3△H3).
(2)某可逆反应:X(g)+3Y(g)?2Z(g)平衡常数与温度关系如表所示:
①根据上述数据判断,该可逆反应的正反应是放热(填“吸热”或“放热”)反应,理由是温度升高,平衡常数减小.
②为了增大X的转化率和反应速率,宜采用的措施是B.
A.升高温度 B.增大压强 C.加催化剂 D.分离Z
③在2L密闭容器中充入Z气体,在一定条件下进行反应.下列图1象不能表明该反应达到平衡状态的是A.

④440℃时,在2L密闭容器中,开始充入1mol X气体和3mol Y气体进行反应.在某时刻测得c(X)=0.45mol/L,此时,反应是否达到平衡状态否(填“是”或“否”),简述理由:此时浓度商Q=$\frac{{c}^{2}(Z)}{c(X){c}^{3}(Y)}$=$\frac{0.{1}^{2}}{0.45×1.3{5}^{3}}$=0.0090<K,平衡正向进行.
⑤在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图2所示(曲线I为标准):
ⅰ曲线Ⅱ改变的条件是升温.
ⅱ曲线Ⅲ改变的条件是加合适的催化剂.
①H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)═S(g)+H2O(g)△H3
④2S(g)═S2(g)△H4
则△H4的正确表达式为$\frac{2}{3}$(△H1+△H2-3△H3).
(2)某可逆反应:X(g)+3Y(g)?2Z(g)平衡常数与温度关系如表所示:
| 温度/℃ | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
②为了增大X的转化率和反应速率,宜采用的措施是B.
A.升高温度 B.增大压强 C.加催化剂 D.分离Z
③在2L密闭容器中充入Z气体,在一定条件下进行反应.下列图1象不能表明该反应达到平衡状态的是A.

④440℃时,在2L密闭容器中,开始充入1mol X气体和3mol Y气体进行反应.在某时刻测得c(X)=0.45mol/L,此时,反应是否达到平衡状态否(填“是”或“否”),简述理由:此时浓度商Q=$\frac{{c}^{2}(Z)}{c(X){c}^{3}(Y)}$=$\frac{0.{1}^{2}}{0.45×1.3{5}^{3}}$=0.0090<K,平衡正向进行.
⑤在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图2所示(曲线I为标准):
ⅰ曲线Ⅱ改变的条件是升温.
ⅱ曲线Ⅲ改变的条件是加合适的催化剂.
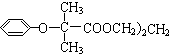
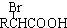 $\stackrel{苯酚钠}{→}$
$\stackrel{苯酚钠}{→}$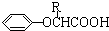
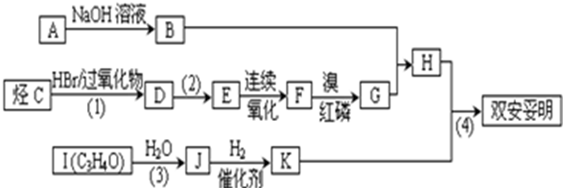
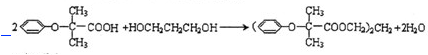
 .
.