题目内容
18.反应4A(g)+5B(g)=4C(g)+6D(g)在0.5L密闭容器中进行,30s内A减少了0.90mol,则此反应的速率可表示为( )| A. | v(B)=0.075mol/(L•s) | B. | v(A)=0.030mol/(L•s) | C. | v(C)=0.040mol/(L•s) | D. | v(D)=0.060mol/(L•s) |
分析 根据v=$\frac{\frac{△n}{V}}{△t}$计算v(A),再利用速率之比等于化学计量数之比计算其它物质表示的速率.
解答 解:在0.5L密闭容器中进行,30s内A减少了0.90mol,则v(A)$\frac{\frac{0.9mol}{0.5L}}{30s}$=0.06mol/(L.s),
速率之比等于化学计量数之比,则:v(B)=$\frac{5}{4}$v(A)=$\frac{5}{4}$×0.06mol/(L.s)=0.075mol/(L.s),
v(C)=v(A)=0.06mol/(L.s),
v(D)=$\frac{6}{4}$v(A)=$\frac{6}{4}$×0.06mol/(L.s)=0.09mol/(L.s),
故选:A.
点评 本题考查化学反应速率有关计算,比较基础,注意对公式的理解与灵活应用,知道反应速率与计量数的关系.

练习册系列答案
相关题目
8.酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法.现用0.1000mol•L-1的标准盐酸去滴定20.00mL 某未知浓度的NaOH溶液,请填写下列空白:
1有关数据记录如下:
该待测NaOH溶液的物质的量浓度是0.10mol•L-1
(2)若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将偏高(选填“偏高”、“偏低”或“不影响”).若读数时,滴定前仰视,滴定后俯视,则测定结果将偏低.
1有关数据记录如下:
| 测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.52 |
| 2 | 20.00 | 1.20 | 21.18 |
| 3 | 20.00 | 0.80 | 24.20 |
(2)若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将偏高(选填“偏高”、“偏低”或“不影响”).若读数时,滴定前仰视,滴定后俯视,则测定结果将偏低.
9.关于下列各实验装置的叙述,不正确的是( )
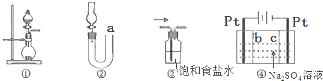

| A. | 图①可用于实验室制取少量NH3或O2 | |
| B. | 可用从a处加水的方法检验图②装置的气密性 | |
| C. | 实验室可用图③的方法除去Cl2中混有的HCl | |
| D. | 利用图④装置制硫酸和氢氧化钠,其中b为阳离子交换膜 |
13.元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z基态原子的2p轨道上有3个未成对电子.下列说法正确的是( )
| A. | X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有12mol σ键 | |
| B. | Z的最高价含氧酸分子中,羟基氧和非羟基氧个数比为1:1 | |
| C. | Y的气态氢化物分子中H-Y-H键角比Y的最高价氧化物分子中O-Y-O键角小 | |
| D. | Z的气态氢化物比Y的气态氢化物稳定,是因为氢键的影响 |
3.有A、B、C、D四块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,外电路电流由D到C;
③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.
据此,判断四种金属的活动性顺序是( )
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,外电路电流由D到C;
③A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应.
据此,判断四种金属的活动性顺序是( )
| A. | A>C>D>B | B. | A>B>C>D | C. | C>A>D>B | D. | C>B>D>A |
10.在一定温度下,反应A2(g)+B2(g)$\stackrel{.}{?}$2AB(g)达到平衡状态的标志是( )
| A. | 单位时间里生成 n mol A2,同时消耗 2n mol AB | |
| B. | 容器中的总压强不随时间而变化 | |
| C. | A2、B2、AB的物质的量之比满足1:1:2 | |
| D. | 单位时间里生成2n mol AB的同时生成n mol B2 |
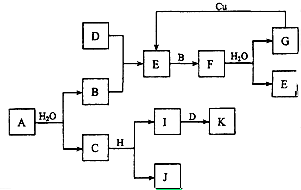 A~K为中学化学的常见物质,它们之间有如下图所示的转化关系(反应条件已略去).已知:通常状况下,A是淡黄色固体,B、D和I都是无色气体单质,F是红棕色气体,H是金属单质.回答下列问题:
A~K为中学化学的常见物质,它们之间有如下图所示的转化关系(反应条件已略去).已知:通常状况下,A是淡黄色固体,B、D和I都是无色气体单质,F是红棕色气体,H是金属单质.回答下列问题: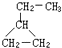 可表示为
可表示为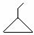 ,则金刚乙烷、金刚乙胺的结构简式可用如图
,则金刚乙烷、金刚乙胺的结构简式可用如图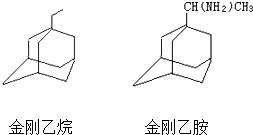 表示.
表示.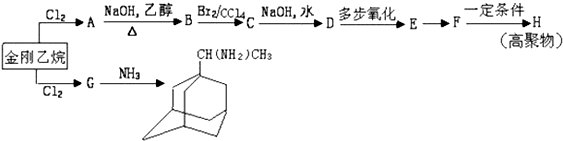
 +2NH3→
+2NH3→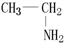 +NH4Cl
+NH4Cl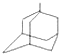 ,如金刚乙烷表示为R-CH2CH3)
,如金刚乙烷表示为R-CH2CH3)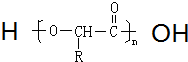 .
.