题目内容
10.在一定温度下,反应A2(g)+B2(g)$\stackrel{.}{?}$2AB(g)达到平衡状态的标志是( )| A. | 单位时间里生成 n mol A2,同时消耗 2n mol AB | |
| B. | 容器中的总压强不随时间而变化 | |
| C. | A2、B2、AB的物质的量之比满足1:1:2 | |
| D. | 单位时间里生成2n mol AB的同时生成n mol B2 |
分析 化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答 解:A.单位时间生成nmol的A2为逆反应,同时生成nmol的AB是正反应,但化学反应速率之比与化学计量数之比不等,故正逆反应速率不等,故A错误;
B.反应前后气体的体积不等,故容器总压强不随时间改变不可作为判断是否达到化学平衡状态的依据,故B错误;
C.平衡时各物质多少决定于开始加入的多少和反应程度,与平衡状态无关,其不能作为判断是否达到化学平衡状态的依据,故C错误;
D.单位时间生成2nmol的AB为正反应,同时生成nmol的B2是逆反应,其速率之比等于化学计量数之比,说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
点评 本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.咖啡酸的结构简式为,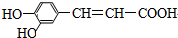
现有①氯化氢 ②溴水 ③纯碱溶液 ④2-丙醇 ⑤酸化的高锰酸钾溶液 ⑥新制氢氧化铜悬浊液.试根据其结构特点判断在一定条件下能与咖啡酸反应的物质组合是( )
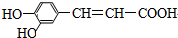
现有①氯化氢 ②溴水 ③纯碱溶液 ④2-丙醇 ⑤酸化的高锰酸钾溶液 ⑥新制氢氧化铜悬浊液.试根据其结构特点判断在一定条件下能与咖啡酸反应的物质组合是( )
| A. | 只有②④⑤⑥ | B. | 只有①③④⑥ | C. | 只有①②③⑤ | D. | ①②③④⑤⑥ |
18.反应4A(g)+5B(g)=4C(g)+6D(g)在0.5L密闭容器中进行,30s内A减少了0.90mol,则此反应的速率可表示为( )
| A. | v(B)=0.075mol/(L•s) | B. | v(A)=0.030mol/(L•s) | C. | v(C)=0.040mol/(L•s) | D. | v(D)=0.060mol/(L•s) |
5.定容容器中反应:N2(g)+3H2(g)?2NH3(g),下列措施不能提高其反应速率的是( )
| A. | 升高温度 | B. | 使用催化剂 | ||
| C. | 充入稀有气体,增大体系压强 | D. | 增加N2和H2的起始量 |
20.下列可设计成原电池的化学反应是( )
| A. | H2O (l)+CaO(s)═Ca(OH)2(s) | |
| B. | Ba(OH)2•8H2O+2NH4Cl═BaCl2+2NH3•H2O+8H2O | |
| C. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ | |
| D. | CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$CO2(g)+2H2O(l) |
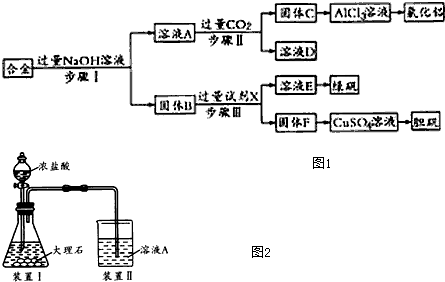
 ) 4种有机物分别在一定条件下与H2充分反应.
) 4种有机物分别在一定条件下与H2充分反应. 滴入溴水后,反应生成产物的结构简式为
滴入溴水后,反应生成产物的结构简式为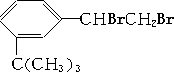 .
.