题目内容
10.下列关于电解质、非电解质的说法正确的是( )| A. | 氯化氢溶于水生成盐酸,盐酸是电解质,氯化氢是非电解质 | |
| B. | NH3 溶于水生成NH3•H2O,NH3•H2O是电解质,NH3是非电解质 | |
| C. | 电解质的水溶液一定能导电,非电解质的水溶液一定不能导电 | |
| D. | 液态CH3COOH不能导电,所以醋酸是非电解质 |
分析 A、溶于水或熔融状态下导电的化合物为电解质;
B、溶于水或熔融状态下导电的化合物为电解质,本身能电离出自已移动的离子;
C、难溶于水的电解质不一定导电,非电解质溶液一定不导电;
D、液态CH3COOH溶于水能导电,属于电解质.
解答 解:A、溶于水或熔融状态下导电的化合物为电解质,氯化氢溶于水生成盐酸,盐酸是氯化氢气体的水溶液,不是电解质,氯化氢是电解质,故A错误;
B、溶于水或熔融状态下导电的化合物为电解质,本身能电离出自已移动的离子,NH3 溶于水生成NH3•H2O,NH3•H2O是电解质,NH3是非电解质,故B正确;
C、难溶于水的电解质不一定导电,如硫酸钡在水溶液中导电性很差,非电解质溶液一定不导电,故C错误;
D、液态CH3COOH溶于水能导电,液态醋酸属于电解质,故D错误;
故选B.
点评 本题考查了电解质、非电解质概念分析,溶液导电性的理解应用,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
1.已知H2S能被下列物质氧化,各物质发生下列变化:Fe3+→Fe2+;Cr2O${\;}_{7}^{2-}$→2Cr3+;Br2→2Br-;HNO3→NO.如果氧化等物质的量的H2S气体得到S单质,需要上述离子或物质的物质的量最小的是( )
| A. | Fe3+ | B. | Cr2O${\;}_{7}^{2-}$ | C. | Br2 | D. | HNO3 |
18.2gAO32-的核外电子数比质子数多3.01×1022个,则A的相对原子质量为( )
| A. | 12 | B. | 32 | C. | 60 | D. | 80 |
15.下列反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | 向漂白粉溶液中加入过量浓盐酸:ClO-+H+=HClO | |
| C. | “万能还原剂”NaBH4与水反应得到NaBO2:BH4-+2H2O=BO2-+4H2↑ | |
| D. | 向FeSO4溶液中加入Na2O2:2Na2O2+2Fe2++2H2O=4Na++2Fe(OH)2↓+O2↑ |
8.硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的流程如图1:

已知:某些氢氧化物沉淀的pH如表所示:
根据题意回答第(1)~(6)题:
(1)在酸解过程中,欲加快酸解时的化学反应速率,请提出两种可行的措施:适当升温、把硼镁泥粉碎或搅拌、或适当增加硫酸浓度.
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,并发生水解,该反应的离子方程式为2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+.
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2、CaSO4.
(4)已知MgSO4、CaSO4的溶解度如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤是蒸发浓缩,趁热过滤.“操作I”是将滤液继续蒸发浓缩,冷却结晶,过滤洗涤,便得到了MgSO4•7H2O.
(5)实验中提供的硼镁泥共100g,得到的MgSO4•7H2O为172.2g,计算MgSO4•7H2O的产率为70%.(保留两位有效数字)
(6)金属镁可用于自然水体中铁件的电化学防腐,完成图2防腐示意图,并作相应标注 和
和 .
.

已知:某些氢氧化物沉淀的pH如表所示:
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
(1)在酸解过程中,欲加快酸解时的化学反应速率,请提出两种可行的措施:适当升温、把硼镁泥粉碎或搅拌、或适当增加硫酸浓度.
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,并发生水解,该反应的离子方程式为2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+.
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2、CaSO4.
(4)已知MgSO4、CaSO4的溶解度如表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(5)实验中提供的硼镁泥共100g,得到的MgSO4•7H2O为172.2g,计算MgSO4•7H2O的产率为70%.(保留两位有效数字)
(6)金属镁可用于自然水体中铁件的电化学防腐,完成图2防腐示意图,并作相应标注
 和
和 .
.
9.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14.X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族.下列说法正确的是( )
| A. | Y分别与X、Z形成的化合物中化学键类型相同 | |
| B. | 原子半径的大小顺序:r(Z)>r(W)>r(Y) | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | Z的最高价氧化物对应的水化物是酸 |
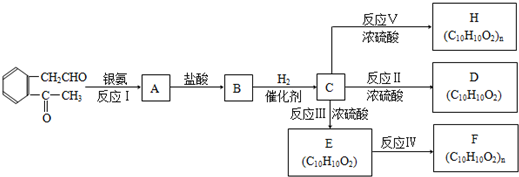
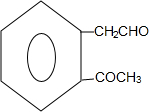 +2Ag(NH3)2OH→
+2Ag(NH3)2OH→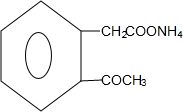 +2Ag↓+3NH3+H2O;
+2Ag↓+3NH3+H2O;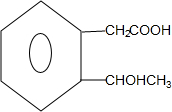 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$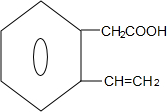 +H2O
+H2O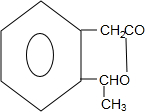 F
F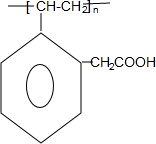 H
H