题目内容
有人建议将氢元素排在元素周期表的ⅦA族.下列事实能支持这一观点的是( )
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H-H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键.
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H-H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键.
| A、①②③ | B、①③④ |
| C、②③④ | D、①②③④ |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据ⅦA族元素原子在反应中易获得一个电子,在化合物中元素的化合价为-1价,易形成离子化合物,以此来解答.
解答:
解:①H原子得到一个电子实现最外电子层稳定结构,在化合物中元素的化合价为-1价,符合ⅦA族元素的化合价,故①正确;
②氢分子的结构式为H-H,符合ⅦA族元素各提供1个电子形成一对共用电子对,故②正确;
③与碱金属元素形成离子化合物M+[:H]-,符合ⅦA族元素与碱金属形成离子化合物的特点,故③正确;
④同种元素原子之间形成非金属性,如氧气、氮气分子都是非极性键,分子中原子间的化学键都属于非极性键不支持氢元素排在元素周期表的ⅦA族的观点,故④错误;
故选A.
②氢分子的结构式为H-H,符合ⅦA族元素各提供1个电子形成一对共用电子对,故②正确;
③与碱金属元素形成离子化合物M+[:H]-,符合ⅦA族元素与碱金属形成离子化合物的特点,故③正确;
④同种元素原子之间形成非金属性,如氧气、氮气分子都是非极性键,分子中原子间的化学键都属于非极性键不支持氢元素排在元素周期表的ⅦA族的观点,故④错误;
故选A.
点评:本题考查原子结构与元素性质,明确ⅦA族元素的性质,寻找H元素与ⅦA族元素性质的共同点,难度不大.

练习册系列答案
相关题目
9g二氧化碳和一氧化碳组成的混合气体与一定量O2恰好完全反应后得到二氧化碳5.6L(标准状况),下列说法正确的是( )
| A、反应前CO和CO2的体积比为1:1 |
| B、反应前CO和CO2的质量比为1:1 |
| C、反应前CO和CO2的混合气体与反应后气体体积比(同温同压下)为1:2 |
| D、反应前CO和CO2的混合气体与反应后气体所含氧原子的个数比为1:2 |
下列与实验相关的叙述正确的是( )
| A、测定中和热时,应将NaOH溶液分次缓慢倒入装有盐酸的烧杯中,并搅拌 |
| B、配置溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、酸碱滴定时,若加入待测前用待测液润洗锥形瓶,将导致测定结果偏高 |
| D、检验某溶液是否含有SO42-时,应取少量溶液,依次加入BaCl2溶液和稀盐酸 |
常温下,0.01mol?L-1 MOH溶液的pH为10.已知:
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
| A、+33.1kJ?mol-1 |
| B、+45.2kJ?mol-1 |
| C、-81.5kJ?mol-1 |
| D、-33.1kJ?mol-1 |
化学学习方法中的类推法是由已学知识通过迁移构建新知识的方法.下列类比正确的是( )
| A、锌可以写溶液中的银离子发生置换反应,钠也能与溶液中的银离子发生置换反应 |
| B、钠与乙醇反应产生氢气,钾与乙醇也能反应产生氢气 |
| C、铜在氯气中剧烈燃烧生成二价铜,铜也能在硫蒸气中剧烈燃烧生成二价铜 |
| D、铜与浓硝酸可以制取NO2,常温下铁与浓耙酸也可以制取NO2 |
下列物质不属于天然高分子化合物的是( )
| A、淀粉 | B、蚕丝 | C、油脂 | D、纤维素 |
下列化学用语正确的是( )
A、氯化氢的电子式: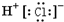 |
B、镁的原子结构示意图: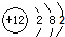 |
| C、乙酸的结构简式 C2H4O2 |
| D、碳酸钠的电离方程式 NaHCO3═Na++H++CO32- |
将0.5mol Na投入过量的水(m1g)中,得到a g溶液;将0.5mol Zn投入过量的盐酸(m2g)中,得到bg溶液,若m1═m2,则a.b的质量关系是( )
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |