题目内容
下列反应的离子方程式书写正确的是( )
A、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+2HCO
| ||
| B、氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+═Fe3++3H2O | ||
C、向亚硫酸钠溶液中加入足量硝酸:SO
| ||
| D、铜溶解于氯化铁溶液中:2Fe3++Cu═2Fe2++Cu2+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成碳酸钡、一水合氨和水;
B.二者发生氧化还原反应生成碘和亚铁离子;
C.二者反应生成硫酸钠和NO;
D.二者反应生成氯化亚铁和氯化铜.
B.二者发生氧化还原反应生成碘和亚铁离子;
C.二者反应生成硫酸钠和NO;
D.二者反应生成氯化亚铁和氯化铜.
解答:
解:A.二者反应生成碳酸钡、一水合氨和水,离子方程式为Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3.H2O+H2O,故A错误;
B.二者发生氧化还原反应生成碘和亚铁离子,离子方程式为2Fe(OH)3+3H++2I-═2Fe2++3H2O+I2,故B错误;
C.二者反应生成硫酸钠和NO,离子方程式为3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O,故C错误;
D.二者反应生成氯化亚铁和氯化铜,离子方程式为2Fe3++Cu═2Fe2++Cu2+,故D正确;
故选D.
B.二者发生氧化还原反应生成碘和亚铁离子,离子方程式为2Fe(OH)3+3H++2I-═2Fe2++3H2O+I2,故B错误;
C.二者反应生成硫酸钠和NO,离子方程式为3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O,故C错误;
D.二者反应生成氯化亚铁和氯化铜,离子方程式为2Fe3++Cu═2Fe2++Cu2+,故D正确;
故选D.
点评:本题考查了离子方程式正误判断,涉及氧化还原反应,明确物质的性质及物质之间的反应是解本题关键,注意碘离子和铁离子不能共存、亚硫酸根离子易被硝酸氧化,为易错点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列叙述正确的是( )
| A、氮在自然界的循环过程中存在形式既有游离态又有化合态,但化合态中没有铵盐 |
| B、按照分散质和分散剂所处状态的不同可以把分散系分为9种类型 |
| C、能使品红溶液褪色的气体一定是SO2 |
| D、某无色溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液-定含有SO42- |
反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )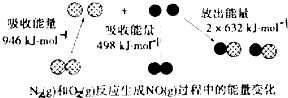
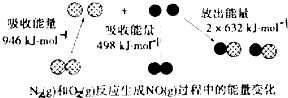
| A、通常情况下,N2(g)和O2(g)混合能直接生成NO |
| B、1mol N2(g)和NA个O2(g)反应放出的能量为180kJ |
| C、NO是一种酸性氧化,能与NaOH溶液反应生成盐和水 |
| D、1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 |
将1000mL 0.1mol?L-1 BaCl2溶液与足量稀硫酸充分反应放出a kJ热量;将1000mL 0.5mol?L-1 HCl溶液与足量CH3COONa溶液充分反应放出b kJ热量(不考虑醋酸钠水解);将500mL 1mol?L-1 H2SO4溶液与足量(CH3COO)2Ba(可溶性强电解质)溶液反应放出的热量为( )
| A、(5a-2b)kJ |
| B、(2b-5a)kJ |
| C、(5a+2b)kJ |
| D、(10a+4b)kJ |
已知破坏1mol H-H键、Cl-Cl键、H-Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与Cl2生成1mol HCl总的过程需要( )
| A、放热185 kJ |
| B、吸热185 kJ |
| C、放热92.5 kJ |
| D、吸热92.5 kJ |
下列说法正确的是( )
| A、铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
| B、硅在电子工业中是最重要的半导体材料,广泛用于制作光导纤维 |
| C、二氧化硫是一种有毒气体,所以不能用于杀菌消毒 |
| D、氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |
9g二氧化碳和一氧化碳组成的混合气体与一定量O2恰好完全反应后得到二氧化碳5.6L(标准状况),下列说法正确的是( )
| A、反应前CO和CO2的体积比为1:1 |
| B、反应前CO和CO2的质量比为1:1 |
| C、反应前CO和CO2的混合气体与反应后气体体积比(同温同压下)为1:2 |
| D、反应前CO和CO2的混合气体与反应后气体所含氧原子的个数比为1:2 |
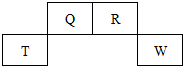 短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )| A、离子半径:Tm+>Wn- |
| B、非金属性:Q<W |
| C、R的氢化物的水溶液呈酸性 |
| D、Q的氧化物都是酸性氧化物 |
常温下,0.01mol?L-1 MOH溶液的pH为10.已知:
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
| A、+33.1kJ?mol-1 |
| B、+45.2kJ?mol-1 |
| C、-81.5kJ?mol-1 |
| D、-33.1kJ?mol-1 |