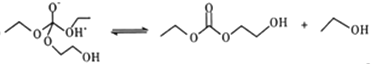
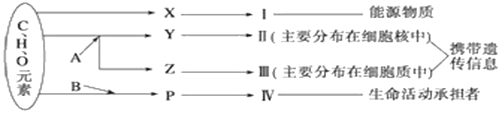
��Ŀ����
����Ŀ������ϸ������������ˮ����NO2��SO2�Ļ�ѧ��Ӧ�ǵ�ǰ�����ڼ������ε���Ҫ����·����ijʵ��С��������ijɷֽ�������֤�����ⶨ������SO2�ĺ�����̽��H2SO3�IJ������ʡ�
�ش�����������
��1���������ij��PM2.5��������Ҫ�ɷ֣��ռ�һ�������������������֤��
ȡһ�����������������Թ��У�����������ˮ�ܽ⣬����Һ�ֳ�����ʢ���Թ���:
�������� | ʵ������ | ���� |
��������һ��_______ | �а�ɫ�������� | ֤�����������к���SO42- |
������һ����_____�������Ӽг�ʪ��ĺ�ɫʯ����ֽ�����Թܿ� | ���Թ��������ݲ�����___________________ | ֤�����������к���NH4+���ۺ�����ʵ��,����˵���������ݿ����к���(NH4)2SO4 |
��2������ͼ��ʾ����װ�òⶨ������SO2�ĺ�����
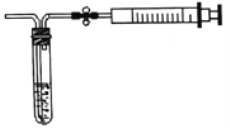
���ⶨԭ����SO2ͨ���ĵ�����Һ�У�ʹ��Һ����ɫ��Ϊ��ɫ����Ӧ�Ļ�ѧ����ʽΪ______��
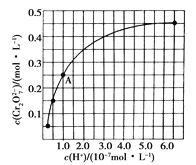
���ⶨ��������ij���㣬��ȡ5.0mL5.0��10-4mol/L�ĵ���Һ��ע��ͼ�е��Թ��У���2-3�ε���ָʾ������ʱ��Һ����ɫ����ͼ��װ�����Ӻ�����������ֹˮ�п��ƣ����г�����ȡ��ע�����������ظ�����ֱ����Һ����ɫȫ���ʾ�Ϊֹ������ȡ����8000.0mL�����øü��������SO2�ĺ���Ϊ_____mg/L��
��3��̽��H2SO3�IJ������ʡ�
ѡ�������װ�ú�ҩƷ̽��H2SO3��HClO������ǿ��
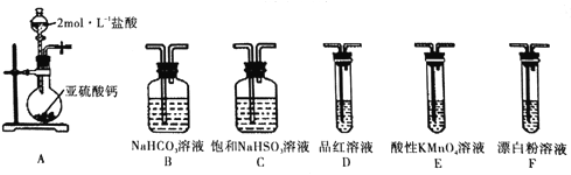
�ټ�ͬѧ��Ϊ����A��C��F��β��������˳������װ�ã�����֤��H2SO3��HClO������ǿ������ͬѧ��Ϊ�÷�������������������_________________��
�ڱ�ͬѧ���ü�ӷ�֤����ʵ�鷽��Ϊ������A��C____(����ĸ) ��β������˳������װ�ã�����װ��C��������___________��֤��H2SO3������ǿ��HClO�����Ե�ʵ��������_____��
���𰸡� ��������ϡ������ټ���BaCl2��Һ ����������NaOHŨ��Һ������ �����Թܿڵĺ�ɫʯ����ֽ����ɫ SO2+I2+2H2O��H2SO4+2HI 0.020 ��������ͨ����������Һ������������ԭ��Ӧ B��E��D��F ��ȥHCl�����������ʵ�� D��Ʒ�첻��ɫ��F�г��ְ�ɫ����
����������1���ڼ���SO42-ʱ�������Ȼ���֮ǰҪ�ȼ��������ų�CO32-���ӵĸ��ţ����ȼ������ữ���������ټ��Ȼ�����Һ�����ְ�ɫ������˵������SO42-������ij��Һ�к���NH4+�IJ�������Ϊ��ȡ�����������뵽�Թ��У���������������Һ���ȣ����Թܿ���ʪ��ĺ�ɫʯ����ֽ����ų����壬��ֽ�ɺ�������ʴ�Ϊ��
�������� | ʵ������ |
��������ϡ������ټ���BaCl2��Һ | |
����������NaOHŨ��Һ������ | �����Թܿڵĺ�ɫʯ����ֽ����ɫ |
��2����SO2ͨ���ĵ�����Һ�У�ʹ��Һ����ɫ��Ϊ��ɫ�����������������������ᣬ��Ӧ�Ļ�ѧ����ʽΪSO2+I2+2H2O��H2SO4+2HI���ʴ�Ϊ��SO2+I2+2H2O��H2SO4+2HI��
�ڶ��������õ���Һ�����գ�����ʽΪ��SO2+I2+2H2O�T2HI+H2SO4��Ϊ�ⶨ�õؿ����е�SO2���������ĵ�����ʵ���=5.0��10-3 L��5��10-4 molL-1=2.50��10-6 mol�����ݻ�ѧ����ʽ�ɵö�����������ʵ���=2.50��10-6 mol������Ϊ2.50��10-6 mol��64g/mol=1.60��10-4 g=0.160mg���ü��������SO2�ĺ���=![]() =0.020 mg/L���ʴ�Ϊ��0.020��
=0.020 mg/L���ʴ�Ϊ��0.020��
��3���ٰ���A��C��F˳������װ�ã����б��͵����������Ƴ�ȥHCl����������ͨ����������Һ������������ԭ��Ӧ������֤��ǿ���Ʊ������ԭ��������֤��������ʹ����������ǿ�����ʴ�Ϊ����������ͨ����������Һ������������ԭ��Ӧ������֤��ǿ���Ʊ������ԭ����
�ڴ��������ǿ�����ԡ�����������л�ԭ�ԣ��������ö���������������ֱ�ӷ�Ӧ�ж�������������������ǿ��������֤���������Ա�̼��ǿ���ٽ��̼�����Ա�HClOǿ�����ж���Aװ���Ʊ������������������ӷ����Ʊ��Ķ��������л���HCl���ñ��͵����������Ƴ�ȥHCl����ͨ��̼��������Һ��������֤���������Ա�̼��ǿ�������Ը��������Һ������ȥ������̼�еĶ���������Ʒ����Һ���������̼�ж��������Ƿ��������ͨ��F�У���װ������˳��ΪA��C��B��E��D��F������װ��C�������dz�ȥHCl���壬D��Ʒ�첻��ɫ��F�г��ְ�ɫ��������֤�������������ǿ�ڴ����ᣬ�ʴ�Ϊ��B��E��D��F����ȥHCl��������Ӱ������ʵ���ã�װ��D��Ʒ�첻��ɫ��F�г��ְ�ɫ������

����Ŀ���±��г��ˢ١������Ԫ�������ڱ��е�λ�ã�
��A | ��A | |||||||
1 | �� | ��A | ��A | ��A | ��A | ��A | ��A | |
2 | �� | �� | �� | �� | ||||
3 | �� | �� | �� | �� | ||||
�밴Ҫ��ش��������⡣
(1)Ԫ�آܵ�������______��Ԫ�آ������ڱ�������λ��____________����Ԫ��ԭ�ӵ�ʧ���ӵĽǶȿ���Ԫ�آܾ���____________��(������ԡ�������ԭ�ԡ�)��
(2)����̬�⻯����ȶ���������ǿ��˳�����У��ޢܢߵ��⻯���ȶ���__________(д�⻯��Ļ�ѧʽ)��
(3)Ԫ�آߵ�ԭ�ӽṹʾ��ͼ��____________��
(4)д��Ԫ�آ��γɵĵ�����������ȼ�յĻ�ѧ����ʽ______________________����һ��Ӧ��____________(����ȡ��������ȡ�)��Ӧ��
(5)Ԫ�آ�����γɵĻ�������������ո�ʱ�������________ɫ��
(6)�õ���ʽ�ֱ��ʾ��ʾ����Ԫ�صĵ��ʷ�Ӧ�õ��Ļ�������γɹ��̣�
����ܣ�___________________________��
����ߣ�___________________________��