题目内容
13.完全燃烧乙烷、丙烯、丁炔各1mol,需要氧气最多的是丁炔,生成的水的质量相等.1mol某不饱和烃可以和1molCl2发生加成反应,生成2,3-二氯-2-甲基丁烷,该不饱和烃结构简式为(CH3)2C=CH-CH2-CH3,与它具有相同官能团的同分异构体(包括该不饱和烃,不考虑顺反异构)数目为13个.分析 令烃的组成为CxHy,相同物质的量的烃,耗氧量取决于(x+$\frac{y}{4}$),(x+$\frac{y}{4}$),值越大耗氧量越大;
乙烷、丙烯、丁炔的分子式分别为C2H6、C3H6、C4H6,分子中含有的H原子数目相同,根据氢元素守恒可知,物质的量相同生成水的质量相同;
1mol某不饱和烃可以和1molCl2发生加成反应,生成2,3-二氯-2-甲基戊烷,根据加成反应的原理,采取倒推法还原C=C双键,从分子中减掉氯原子形成C=C双键,可得不饱和烃的结构,具有相同官能团的同分异构体个数有1、1-已烯;2、2-甲基1-戍烯;3、3-甲基1-戍烯;4、4-甲基1-戍烯;5、2-甲基2-戍烯;6、3-甲基2-戍烯;7、4-甲基2-戍烯;8、2-已烯;9、3-已烯;10、2、3-二甲基1-丁烯;11、3、3-二甲基1-丁烯;12、2-乙基1-丁烯;13、2、3-二甲基2-丁烯.
解答 解:乙烷分子式为C2H6,其(x+$\frac{y}{4}$)=2+$\frac{6}{4}$=3.5,丙烯的分子式为C3H6,其(x+$\frac{y}{4}$)=3+$\frac{6}{4}$=4.5,丁炔的分子式为C4H6,其(x+$\frac{y}{4}$)=4+$\frac{6}{4}$=5.5,故相同物质的量的烃,丁炔的耗氧量最多;乙烷、丙烯、的分子式分别为C2H6、C3H6、C4H6,分子中含有的H原子数目相同,根据氢元素守恒可知,物质的量相同生成水的质量相同;
1mol某不饱和烃可以和1molCl2发生加成反应,生成2,3-二氯-2-甲基戊烷,根据加成反应的原理,采取倒推法还原C=C双键,从分子中减掉氯原子形成C=C双键,可得不饱和烃的结构为(CH3)2C=CH-CH2-CH3,根据系统命名法命名为2-甲基-2-戊烯,它具有相同官能团的同分异构体13种.
故答案为:丁炔;水;(CH3)2C=CH-CH2-CH3;13.
点评 本题考查烃的耗氧量规律、有机物结构推断、有机物的命名等,难度不大,注意基础知识的掌握,注意本题中由于烃分子中H原子数目相同,耗氧量可以利用碳原子数目越多,耗氧量越多.

 一线名师权威作业本系列答案
一线名师权威作业本系列答案| A. | 纯银饰品久置表面变暗属于化学腐蚀 | |
| B. | 温度越高,金属发生化学腐蚀的速率越快 | |
| C. | 金属腐蚀就是金属失去电子被氧化的过程 | |
| D. | 铁门上的铜铆钉处在潮湿的空气中直接发生反应:Fe-3e-═Fe3+ |
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E元素的+3价离子有5个未成对电子 |
| F在周期表的第15列 |
(2)某同学根据上述信息,所画的
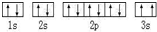 B电子排布图如图,违背了泡利原理.
B电子排布图如图,违背了泡利原理.(3)CD3中心原子的杂化方式为sp3,分子立体构型三角锥形形.
(4)E元素基态原子的电子占用15个原子轨道,有26种不同运动状态.
(5)F元素的元素符号为As,其基态原子的核外电子排布式1s22s22p63s23p63d104s24p3.
| A. | 向氨水中通入HCl气体,溶液导电性增强 | |
| B. | 向氨水中加入水,$\frac{{C}_{(O{H}^{-})}}{N{H}_{3}•{H}_{2}O}$值增大 | |
| C. | 向氨水中通入NH3,电离度增大 | |
| D. | 向氨水中加入水,Kb不变 |
| A. | CH3CH2CH2CH2CH2CH2Br | B. | 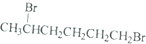 | ||
| C. | 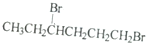 | D. | BrCH2CH2CH2CH2CH2Br |
| A. | 聚乙烯 | B. | 聚丁二烯 | C. | 石油裂化 | D. | 石油裂解 |