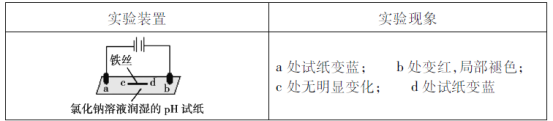
题目内容
【题目】下列说法正确的是( )
A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则△H<0
B.铁片镀锌时,铁片与外电源的正极相连
C.以熔融NaCl为电解质进行电解冶炼钠,熔融体中Na+向阳极移动
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)![]() NO(g)+SO3(g),通入少量O2,
NO(g)+SO3(g),通入少量O2,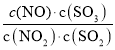 的值及SO2转化率不变
的值及SO2转化率不变
【答案】A
【解析】
A.△H-T△S<0时反应能自发进行,该反应的△S<0,则△H<0,A正确;
B.铁片镀锌时,铁片应接电源负极,作阴极,锌离子在铁片上发生还原反应,B错误;
C.电解时,阳离子向阴极移动,C错误;
D.通入氧气与NO反应,c(NO)减小,平衡正向移动,SO2转化率增大,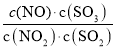 是平衡常数,温度不变,平衡常数不变,D错误。
是平衡常数,温度不变,平衡常数不变,D错误。
答案选A。

练习册系列答案
相关题目