题目内容
【题目】硒(Se)是第四周期ⅥA族元素,是人体内不可或缺的微量元素,其氢化物H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的基础原料。
(1)已知:①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=a kJ·mol1
2Se(s)+2H2O(l) ΔH1=a kJ·mol1
②2H2(g)+O2(g)= 2H2O(l) ΔH2=b kJ·mol1
反应H2(g)+Se(s)![]() H2Se(g)的反应热ΔH3=___________kJ·mol1(用含a、b的代数式表示)。
H2Se(g)的反应热ΔH3=___________kJ·mol1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和lmolSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①下列情况可判断反应达到平衡状态的是___________(填字母)。
a.气体的密度不变 b.υ(H2)=υ(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为液体H2Se,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释_________________________________。
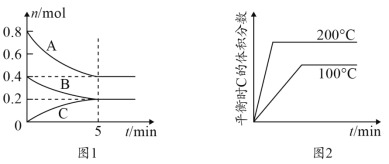
③以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如下图所示:
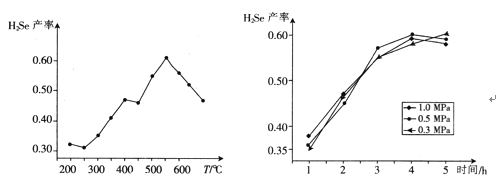
则制备H2Se的最佳温度和压强为______________________。
(3)已知常温下H2Se的电离平衡常数K1=1.3×104,K2=5.0×1011,则NaHSe溶液呈___________(填“酸性”或“碱性”),该溶液中的物料守恒关系式为____________________。
(4)用电化学方法制备H2Se的实验装置如下图所示:
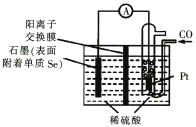
写出Pt电极上发生反应的电极反应式:_________________________________。
(5)H2Se在一定条件下可以制备CuSe,已知常温时CuSe的Ksp=7.9×1049,CuS的Ksp=1.3×1036,则反应CuS(s)+Se2-(aq)![]() CuSe(s)+S2-(aq)的化学平衡常数K=________(保留2位有效数字)。
CuSe(s)+S2-(aq)的化学平衡常数K=________(保留2位有效数字)。
【答案】![]() (ba) ad 将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高 550℃,0.3 MPa 碱性 c(Na+)=c(HSe)+c(Se2)+c(H2Se) CO2e+H2O=CO2+2H+ 1.6×1012
(ba) ad 将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高 550℃,0.3 MPa 碱性 c(Na+)=c(HSe)+c(Se2)+c(H2Se) CO2e+H2O=CO2+2H+ 1.6×1012
【解析】
(1)根据盖斯定律求出反应的H;
(2)①该反应为气体的总物质的量不变的反应,根据反应达到平衡的判断依据作答;
②分离出的H2重新通入反应容器,会增大反应物中H2的浓度,据此分析对平衡的影响效果;
③结合已知图像分析作答;
(3)HSe 在溶液中存在电离平衡和水解平衡,根据已知条件求出HSe的水解平衡常数,进而比较出水解程度与电离程度的相对大小分析,再结合物料守恒作答;
(4)通入CO的Pt电极为原电池的负极,依据原电池原理书写其电极反应式;
(5)根据沉淀转化的化学平衡常数与各沉淀溶度积之间的关系进行计算。
(1)根据盖斯定律可知ΔH3 =![]() (ΔH2ΔH1)=
(ΔH2ΔH1)=![]() (ba)kJ·mol1,
(ba)kJ·mol1,
故答案为![]() (ba);
(ba);
(2)①由于反应前后气体的质量发生了变化,但气体的总物质的量不变,则
a. 建立平衡过程中气体质量增加,容器体积不变,气体密度增大,达到平衡时气体质量不变、气体密度不变,气体的密度不变能说明反应达到平衡状态;
b. υ(H2)= υ(H2Se)没有指明反应速率的方向,υ(H2)= υ(H2Se)不能作为达到平衡的判定依据;
c. 反应过程中在任何时刻压强都不改变,所以压强不变不能作为反应达到平衡的判定依据;
d. 建立平衡过程中气体质量增加,气体物质的量不变,气体的平均摩尔质量增大,达到平衡时气体质量不变,气体的平均摩尔质量不变,气体的平均摩尔质量不变能说明反应达到平衡状态;
故答案为ad;
②将平衡混合气通入气体液化分离器气体H2Se转化为液体H2Se,并将分离出的H2重新通入反应容器,会增大反应物中H2的浓度,平衡正向移动,Se的转化率提高,
故答案为将分离出的H2重新通入容器中,平衡正向移动,Se的转化率提高;
③由于最终是以5小时内得到的H2Se为产量指标,则从图1可知,在550℃时产率最高,所以最适宜的反应温度为550 ℃;由图2可知,反应5小时左右时,压强为0.3 Mpa条件下产率最高,因此最适宜压强为0.3 Mpa,
故答案为550℃,0.3 MPa;
(3)HSe 在溶液中存在电离平衡和水解平衡,HSe的水解平衡常数 = ![]() ≈7.7×1011>K2=5.0×1011,即HSe的水解能力大于其电离能力,则NaHSe溶液呈碱性,溶液中的物料守恒关系为c(Na+)=c(HSe)+c(Se2)+c(H2Se),
≈7.7×1011>K2=5.0×1011,即HSe的水解能力大于其电离能力,则NaHSe溶液呈碱性,溶液中的物料守恒关系为c(Na+)=c(HSe)+c(Se2)+c(H2Se),
故答案为碱性;c(Na+)=c(HSe)+c(Se2)+c(H2Se);
(4)根据题意,结合装置图,石墨极上Se得到电子发生还原反应生成H2Se,则石墨为正极,Pt为负极,在Pt电极上CO失电子发生氧化反应,电极反应式为CO2e+H2O=CO2+2H+,
故答案为CO2e+H2O=CO2+2H+;
(5)反应CuS(s)+Se2(aq)![]() CuSe(s)+S2(aq)的化学平衡常数K=
CuSe(s)+S2(aq)的化学平衡常数K= =
= =
= =
=![]() ≈1.6×1012,
≈1.6×1012,
故答案为1.6×1012。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】碘在科研与生活中有重要应用。
(1)I2O5 是白色粉末状固体,在合成氨工业中常用 I2O5 来定量测量 CO 的含量。
已知:2I2 (s)+5O2 (g)=2I2O5 (s) △H=﹣75.56kJ·mol-1
2CO (g)+O2 (g)=2CO2 (g) △H=﹣566.0kJ·mol-1
写出 CO (g)与 I2O5 (s)反应析出固态 I2 的热化学方程式:_____,若这个反应一定能自发进行,则反应的△S_____0(填“>”,“<”或 “=”);
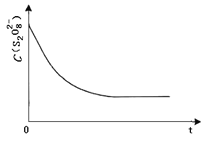
(2)某兴趣小组用 0.50mol·L-1KI、0.2%淀粉溶液、0.20mol·L-1K2S2O8、0.10mol·L-1Na2S2O3 等试 剂,探究反应条件对化学反应速率的影响。
已知:Ⅰ、S2O82-+2I-=2SO42-+I2(慢) Ⅱ、I2+2S2O32-=2I- +S4O62-(快)
①向 KI、Na2S2O3 与淀粉的混合溶液中加入一定量的 K2S2O8 溶液,当溶液中的_____耗 尽后,溶液颜色将由无色变成为蓝色。 请从碰撞理论的角度解释上述产物未耗尽前溶液中看不到蓝色的原因:_____
②为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 序号 | 体积 V/mL | ||||
K2S2O8 溶液 | 水 | KI 溶液 | Na2S2O3 溶液 | 淀粉溶液 | |
ⅰ | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
ⅱ | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
ⅲ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
表中 Vx=_____mL,理由是_____。
③已知某条件下,浓度 c (S2O82-)~反应时间 t 的变化曲线如图,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时 c (S2O82-)~t 的变化曲线示意图 _____(进行相应的标注)