题目内容
【题目】有机物K是某药物的合成中间体,其合成路线如图所示:

已知:①HBr与不对称烯桂加成时,在过氧化物作用下,则卤原子连接到含氢较多的双键碳上;
②R—CN![]() R-CH2NH2(R表示坯基);
R-CH2NH2(R表示坯基);
③R1—CN2+R-COOC2H5![]()
![]() +C2H5OH(R表示烃基或氢原子)。
+C2H5OH(R表示烃基或氢原子)。
请回答下列问题:
(1)C的化学名称为_______________。
(2)D→E的反应类型为_________,F中官能团的名称是____________。
(3)G→H的化学方程式为____________________。
(4)J的分子式为__________________。手性碳原子是指与四个各不相同原子或基团相连的碳原子,则K分子中的手性碳原子数目为_______。
(5)L是F的同分异构体,则满足下列条件的L的结构简式为____________。(任写一种结构即可)
①lmolL与足量的NaHCO3溶液反应能生成2molCO2;
②L的核磁共振氢谱有3组峰且峰面积之比为1:2:3。
(6)请写出J经三步反应合成K的合成路线:____________________(无机试剂任选)。
【答案】1,3-二溴丙烷 氧化反应 酯基 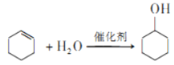 C13H20O4 1
C13H20O4 1 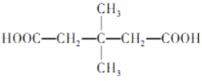 或
或
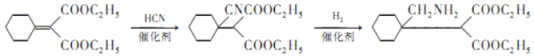

【解析】
A:CH3CH=CH2在光照、加热条件下与溴发生取代反应生成B为CH2BrCH=CH2,CH2BrCH=CH2在过氧化物作用下,与HBr发生加成反应生成C为CH2BrCH2CH2Br,CH2BrCH2CH2Br在氢氧化钠水溶液中加热发生水解反应生成D为HOCH2CH2CH2OH,HOCH2CH2CH2OH被酸性高锰酸钾氧化生成E为HOOCCH2COOH,HOOCCH2COOH在浓硫酸催化下与乙醇发生酯化反应生成F为CH3CH2OOCCH2COOCH2CH3;G水化催化生成H,则G为![]() ,
,![]() 与水发生加成反应生成H,H在催化剂作用下发生氧化反应生成I为
与水发生加成反应生成H,H在催化剂作用下发生氧化反应生成I为![]() ;
;![]() 与CH3CH2OOCCH2COOCH2CH3在一定条件下反应生成J,J经三步反应生成K,据此分析。
与CH3CH2OOCCH2COOCH2CH3在一定条件下反应生成J,J经三步反应生成K,据此分析。
A:CH3CH=CH2在光照、加热条件下与溴发生取代反应生成B为CH2BrCH=CH2,CH2BrCH=CH2在过氧化物作用下,与HBr发生加成反应生成C为CH2BrCH2CH2Br,CH2BrCH2CH2Br在氢氧化钠水溶液中加热发生水解反应生成D为HOCH2CH2CH2OH,HOCH2CH2CH2OH被酸性高锰酸钾氧化生成E为HOOCCH2COOH;G水化催化生成H,则G为![]() ,
,![]() 与水发生加成反应生成H,H在催化剂作用下发生氧化反应生成I为
与水发生加成反应生成H,H在催化剂作用下发生氧化反应生成I为![]() ;
;![]() 与HOOCCH2COOH在一定条件下反应生成J,J经三步反应生成K。
与HOOCCH2COOH在一定条件下反应生成J,J经三步反应生成K。
(1)C为CH2BrCH2CH2Br,化学名称为1,3-二溴丙烷;
(2)D→E 是HOCH2CH2CH2OH被酸性高锰酸钾氧化生成HOOCCH2COOH,反应类型为氧化反应,F 为CH3CH2OOCCH2COOCH2CH3官能团的名称是酯基;
(3)G→H是![]() 水化催化生成
水化催化生成![]() ,的化学方程式为
,的化学方程式为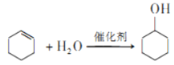 ;
;
(4)J为![]() ,分子式为C13H20O4。手性碳原子是指与四个各不相同原子或基团相连的碳原子,则K(
,分子式为C13H20O4。手性碳原子是指与四个各不相同原子或基团相连的碳原子,则K(![]() )分子中的手性碳原子数目为1(标红色处);
)分子中的手性碳原子数目为1(标红色处);
(5)L是F的同分异构体,满足条件:①lmolL与足量的NaHCO3溶液反应能生成2molCO2,则分子中含有两个羧基;②L的核磁共振氢谱有3组峰且峰面积之比为1:2:3,则高度对称,符合条件的同分异构体有 或
或 ;
;
(6)J经三步反应合成K:![]() 与HCN发生加成反应生成
与HCN发生加成反应生成![]() ,
,![]() 与氢气发生加成反应生成
与氢气发生加成反应生成![]() ,
,![]() 在催化剂作用下转化为
在催化剂作用下转化为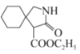 ,合成路线为
,合成路线为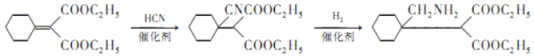
 。
。

 优百分课时互动系列答案
优百分课时互动系列答案