题目内容
7.硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2.850℃~950℃时,硫铁矿在空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4:1):3FeS2+8O2→Fe3O4+6SO2 ①
4FeS2+11O2→2Fe2O3+8SO2 ②
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为65.6%.
(2)设1t纯净的FeS2按②式完全反应,产生标准状况下SO2373.3 m3.
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少?
(4)480g纯净的FeS2在空气中完全反应,若所得固体中,Fe和O的物质的量之比n(Fe):n(O)=4:a,此时消耗空气为bmol.试写出b与a的关系式b=2.5a+40.
分析 (1)硫元素含量=FeS2的含量×FeS2中S元素质量分数;
(2)根据方程式计算生成二氧化硫的体积;
(3)设FeS2为1 mol,计算完全煅烧需要的n(O2)、生成的n(SO2),结合空气中氧气含量计算过量20%所需空气物质的量,计算炉气的物质的量,进而计算SO2体积分数;
(4)bmol空气所含氧气为:n (O2)=0.2bmol,根据S原子守恒计算SO2的物质的量,根据O原子守恒计算固体中O原子物质的量,再结合固体中Fe、O原子数目之比计算.
解答 解:(1)硫元素含量=FeS2的含量×FeS2中S元素质量分数,故FeS2的含量为$\frac{35%}{\frac{64}{120}}$=65.6%,
故答案为:65.6%;
(2)设生成二氧化硫的体积为V m3,则:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
480g 8×22.4L
106g 1000V L
故480g:106g=8×22.4L:1000V L
解得V=373.3,
故答案为:373.3;
(3)设FeS2为1 mol,由4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2 可知,完全煅烧需要的n(O2)=1mol×$\frac{11}{4}$=2.75 mol,生成n(SO2)=2 mol;
过量20%所需空气为:n(空气)=2.75mol÷0.2×1.2=16.5 mol,
SO2体积分数为:SO2%=2mol÷(16.5+2-2.75)mol=12.7%,
答:所得炉气中SO2的体积分数为12.7%;
(4)bmol空气所含氧气为:n (O2)=0.2bmol;480 g纯净的FeS2为$\frac{480g}{120g/mol}$=4mol,完全反应生成8molSO2,故存在于固体中的n (O)=(0.2b-8)×2mol,则:n (Fe):n (O)=4:a=4:(0.2b-8)×2,故b=2.5a+40,
故答案为:b=2.5a+40.
点评 本题考查化学方程式计算,侧重考查学生的分析计算能力,注意对基础知识的理解掌握,难度不大.

| A. | 用托盘天平称量药品时,将药品置于天平右盘 | |
| B. | 蒸馏实验中,要在烧瓶中加入沸石或碎瓷片,以防止液体暴沸 | |
| C. | 用托盘天平称取10.50g干燥的NaCl固体 | |
| D. | 向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体 |
| A. | 3.18 g | B. | 2.12 g | C. | 4.22 g | D. | 5.28 g |
| A. | 液氨中含有NH3、NH4+、NH2-微粒 | |
| B. | 其他条件不变,若增加液氨的量,电离平衡将正向移动 | |
| C. | 只要不加入其他物质,液氨中c(NH4+)=c(NH2-) | |
| D. | 一定温度下液氨中c(NH4+)•c(NH2-)是一个常数 |
 在一定温度下,容器内某一反应中的M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中的M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | t2时,正逆反应速率相等 | B. | t1时,N的浓度是M浓度的2倍 | ||
| C. | t3时,正反应速率大于逆斥速率 | D. | t3时,正反应速率等于逆反应速率 |
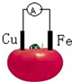
| A. | 铜片为负极 | B. | 铁片上发生还原反应 | ||
| C. | 电子由铁片沿导线流向铜极 | D. | 该装置将电能转变为化学能 |
| A. |  浓硫酸的稀释 | |
| B. | 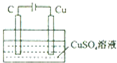 某电极上有铜产生,且溶液中铜离子浓度不变 | |
| C. | 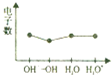 微粒电子数 | |
| D. |  过量的盐酸与等量的锌粉反应 |
| A. | HCl | B. | FeCl2 | C. | CuCl2 | D. | NaCl |