题目内容
16.下列图象表达正确的是( )| A. |  浓硫酸的稀释 | |
| B. | 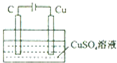 某电极上有铜产生,且溶液中铜离子浓度不变 | |
| C. | 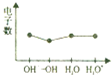 微粒电子数 | |
| D. |  过量的盐酸与等量的锌粉反应 |
分析 A、加水稀释浓硫酸的密度减小;
B、铜与电源的负极相连,电极本身不放电;
C、氢氧根离子、水和水合氢离子都是10电子的微粒,而羟基是9电子的微粒;
D、滴有硫酸铜的体系中,少量的锌与铜离子发生置换反应生成铜,铜与锌构成原电池,反应速率加快,但因铜与盐酸中氢离子不发生反应,所以生成氢气的量变少.
解答 解:A、加水稀释浓硫酸的密度减小,而不是增加,图象与实际不相符,故A错误;
B、铜与电源的负极相连,电极本身不放电,而阴极铜离子放电,所以溶液中铜离子的浓度减少,故B错误;
C、氢氧根离子、水和水合氢离子都是10电子的微粒,而羟基是9电子的微粒,所以图符合,故C正确;
D、滴有硫酸铜的体系中,少量的锌与铜离子发生置换反应生成铜,铜与锌构成原电池,反应速率加快,但因铜与盐酸中氢离子不发生反应,所以生成氢气的量变少,而不是不变,图象与实际不相符,故D错误;
故选C.
点评 本题考查了硫酸的密度、原电池原理的应用、微粒电子数的求算等知识,属于综合知识的考查,侧重于基础知识的应用的考查,难度中等.

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
4.能证明硅酸的酸性比碳酸的酸性弱的实验事实是( )
| A. | CO2通入可溶性硅酸盐中析出硅酸沉淀 | |
| B. | CO2溶于水形成碳酸,SiO2难溶于水 | |
| C. | 高温下SiO2与碳酸盐反应生成CO2 | |
| D. | 氯化氢通入碳酸钠溶液中放出气体,通入硅酸钠溶液中生成沉淀 |
11.下列关于SiO2和CO2的叙述中不正确的是( )
| A. | SiO2的熔点比CO2高 | |
| B. | SiO2用于制光导纤维,干冰用于人工降雨 | |
| C. | 都能与水反应生成相应的酸 | |
| D. | 都能与强碱溶液反应 |
1.下列生活常见现象中,没有涉及化学变化的是( )
| A. | 钢铁生锈 | B. | 海水晒盐 | C. | 食物腐败 | D. | 臭氧消毒 |
8.下列有关离子方程式表达正确的是( )
| A. | 实验室制备氢气:Cu+2H+═Cu2++H2↑ | |
| B. | NaOH溶液不能用带玻璃塞的试剂瓶保存:SiO2+2OH-═SiO32-+H2O | |
| C. | CuSO4和Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ | |
| D. | CO2通入氯化钙溶液中:Ca2++CO2+H2O═CaCO3↓+2H+ |
5.下列关于胶体的叙述不正确的是( )
| A. | 胶体是一种混合物 | |
| B. | 利用丁达尔效应可以区分溶液和胶体 | |
| C. | 胶体是一种介稳体系 | |
| D. | 大小介于1~100 nm 之间的微粒称为胶体 |
6.下列各组离子中,能够大量共存且加入稀硫酸会产生气体的是( )
| A. | Fe3+、Na+、HCO${\;}_{3}^{-}$、Cl- | B. | Al3+、Na+、Cl-、F- | ||
| C. | Zn2+、K+、Cl-、SO${\;}_{4}^{2-}$ | D. | Fe2+、Na+、Cl-、NO${\;}_{3}^{-}$ |
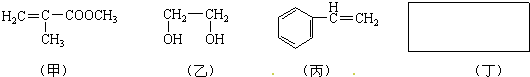
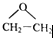 ,该反应的原子利用率为100%,其化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$2
,该反应的原子利用率为100%,其化学方程式为2CH2=CH2+O2$→_{△}^{Ag}$2
 .
.