题目内容
19.如图为铁、铜水果电池装置示意图,下列说法正确的是( )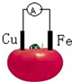
| A. | 铜片为负极 | B. | 铁片上发生还原反应 | ||
| C. | 电子由铁片沿导线流向铜极 | D. | 该装置将电能转变为化学能 |
分析 根据金属的活泼性知,Fe作负极,Cu作正极,负极上Fe失电子发生氧化反应,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,据此解答.
解答 解:A.该原电池中,Fe的活泼性比Cu强,Fe作负极,故A错误;
B.铁为负极,发生氧化反应,故B错误;
C.Fe作负极,铜作正极,电子从Fe沿导线流向Cu,故C正确;
D.形成原电池反应,化学能转化为电能,故D错误.
故选C.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,难度不大,明确电子的移动方向、电极的判断是解题的关键.

练习册系列答案
相关题目
9.下列事实中不能证明CH3COOH是弱电解质的是( )
| A. | 常温下CH3COONa某溶液的pH=8 | |
| B. | 用CH3COOH溶液做导电实验,灯泡很暗 | |
| C. | 等pH等体积的盐酸、CH3COOH溶液分别与足量锌反应,CH3COOH放出的氢气较多 | |
| D. | 0.1mol•L-1的CH3COOH溶液中含有CH3COOH、CH3COO-、H+、OH- |
10.63Li和73Li是锂的两种稳定同位素,在地质学和地球化学研究中有着广阔的应用前景.下列说法正确的是
( )
( )
| A. | 63Li和73Li是同一种核素 | B. | 63Li和73Li的中子数相同 | ||
| C. | 63Li和73Li的电子数相差1 | D. | 63Li和73Li的质子数相同 |
4.能证明硅酸的酸性比碳酸的酸性弱的实验事实是( )
| A. | CO2通入可溶性硅酸盐中析出硅酸沉淀 | |
| B. | CO2溶于水形成碳酸,SiO2难溶于水 | |
| C. | 高温下SiO2与碳酸盐反应生成CO2 | |
| D. | 氯化氢通入碳酸钠溶液中放出气体,通入硅酸钠溶液中生成沉淀 |
11.下列关于SiO2和CO2的叙述中不正确的是( )
| A. | SiO2的熔点比CO2高 | |
| B. | SiO2用于制光导纤维,干冰用于人工降雨 | |
| C. | 都能与水反应生成相应的酸 | |
| D. | 都能与强碱溶液反应 |
8.下列有关离子方程式表达正确的是( )
| A. | 实验室制备氢气:Cu+2H+═Cu2++H2↑ | |
| B. | NaOH溶液不能用带玻璃塞的试剂瓶保存:SiO2+2OH-═SiO32-+H2O | |
| C. | CuSO4和Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ | |
| D. | CO2通入氯化钙溶液中:Ca2++CO2+H2O═CaCO3↓+2H+ |
9.下列反应既属于离子反应,又属于氧化还原反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | ||
| C. | Fe+2HCl=FeCl2+H2↑ | D. | 2NaOH+CO2═Na2CO3+H2O |