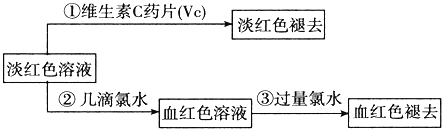
题目内容
【题目】某学习小组用碳素钢进行了以下探究活动:
[探究一](1)将已去除表面氧化膜的碳素钢钉放入冷浓硫酸中,10min后将钢钉浸入CuSO4溶液中,钢钉表面无明显变化,其原因是 ______ .
(2)称取6.0g碳素钢放入15.0ml浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y.
①甲同学认为X中除Fe3+之外还可能含有Fe2+,若要确认是否含有Fe2+,可选用 ______ ![]() 选填序号
选填序号![]() .
.
A.KSCN溶液B.浓氨水C.酸性KMnO4溶液 D.K3[Fe(CN)6]溶液
②乙同学取560ml(标准状况)干燥气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g,由此可知Y中含硫化合物Q1的体积分数为 ______ .
[探究二]丙同学认为气体Y中还可能含有Q2、Q3两种气体(相同条件下Q1、Q2、Q3气体的密度依次减小).为此,设计了下列装置进行实验探究(假设有关气体完全反应).
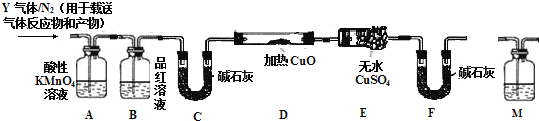
(3)装置B中试剂的作用是 ______ .
(4)已知洗气瓶M中盛装的是澄清石灰水,为确认Q2的存在,洗气瓶M的位置应在 ______ ,产生Q2的反应的化学方程式为 ______ .
(5)确认含有气体Q3的实验现象是 ______ ,产生Q3的反应的离子方程式为 ______ .
【答案】Fe表面被浓硫酸作用发生了钝化,生成了一层氧化物膜 CD 80% 确认SO2已除尽 B与C之间 ![]() 浓
浓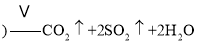 D中固体由黑变红、E中固体由白变蓝
D中固体由黑变红、E中固体由白变蓝 ![]()
【解析】
[探究一](1)常温下,铁易和浓硫酸发生钝化现象,从而阻止进一步反应;
(2)亚铁离子有还原性,能还原酸性高锰酸钾溶液而使其褪色,亚铁离子遇到K3[Fe(CN)6]溶液变蓝色是亚铁离子的特征性质;根据硫酸钡与二氧化硫的关系式计算二氧化硫的体积,再根据体积分数公式计算;
[探究二]称取6.0g碳素钢放入15.0ml浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y,气体Y中还可能含有Q2、Q3两种气体(相同条件下Q1、Q2、Q3气体的密度依次减小),依据反应实质分析可知,浓硫酸和铁反应生成硫酸铁、二氧化硫和水,所含碳和浓硫酸加热反应生成二氧化碳、二氧化硫和水,随反应进行浓硫酸变为稀硫酸和铁反应生成气体为氢气,Q1、Q2、Q3气体成分为SO2、CO2、H2,依据装置通过装置A中高锰酸钾溶液除去二氧化硫,装置B中品红溶液检验二氧化硫是否除净,通过碱石灰吸收二氧化碳、水蒸气,通过装置D加热的氧化铜和氢气发生反应生成铜和水蒸气,进入装置F无水硫酸铜变蓝色,装置F是防止空气中水蒸气进入装置F影响产物检验,
(3)二氧化硫能使品红溶液褪色,据此判断是否含有二氧化硫;
(4)用澄清石灰水检验二氧化碳,首先要排除二氧化硫的干扰;碳素钢中含有碳,加热条件下,碳和浓硫酸反应生成二氧化碳;
(5)浓硫酸随反应进行浓度减小变化为稀硫酸和铁反应生成Q3为氢气;
[探究一](1)常温下,Fe易和浓硫酸发生氧化还原反应生成致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以放入浓硫酸后的碳素钢加入硫酸铜溶液中无变化,说明Fe表面发生了钝化,生成了一层氧化物膜;
(2)①亚铁离子具有还原性,而酸性高锰酸钾有氧化性,发生氧化还原反应使高锰酸钾溶液褪色,亚铁离子遇到K3[Fe(CN)6]溶液变蓝色;
答案选CD;
![]() ,
,![]() ,所以硫酸钡和二氧化硫之间的关系式为SO2 ~ BaSO4,设二氧化硫的体积为V,
,所以硫酸钡和二氧化硫之间的关系式为SO2 ~ BaSO4,设二氧化硫的体积为V,
SO2 ~ BaSO4,
2.24L 233 g
V 4.66g V=0.448l=448ml,
所以二氧化硫的体积分数![]() ;
;
[探究二]称取6.0g碳素钢放入15.0ml浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y,气体Y中还可能含有Q2、Q3两种气体(相同条件下Q1、Q2、Q3气体的密度依次减小),依据反应实质分析可知,浓硫酸和铁反应生成硫酸铁、二氧化硫和水,所含碳和浓硫酸加热反应生成二氧化碳、二氧化硫和水,随反应进行浓硫酸变为稀硫酸和铁反应生成气体为氢气,Q1、Q2、Q3气体成分为SO2、CO2、H2,依据装置通过装置A中高锰酸钾溶液除去二氧化硫,装置B中品红溶液检验二氧化硫是否除净,通过碱石灰吸收二氧化碳、水蒸气,通过装置D加热的氧化铜和氢气发生反应生成铜和水蒸气,进入装置F无水硫酸铜变蓝色,装置F是防止空气中水蒸气进入装置F影响产物检验,
(3)二氧化硫能使品红溶液褪色,所以用品红溶液检验二氧化硫是否除尽;
(4)二氧化硫和二氧化碳都能使澄清石灰水变浑浊,但二氧化硫还能使品红溶液褪色,所以要检验二氧化碳必须排除二氧化硫的干扰,B装置是检验二氧化硫是否除尽,所以澄清石灰水应放置在B和C之间,碳素钢中含有碳,加热条件下,碳能和浓硫酸反应生成二氧化硫、二氧化碳和水,反应方程式为:![]() 浓
浓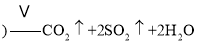 ;
;
(5)确认含有气体![]() 为氢气的实验现象是,氢气还原氧化铜固体黑色变化为红色,生成气体中含水蒸气,遇到无水硫酸铜变蓝色,确认含有气体Q3的实验现象是D中固体由黑变红、E中固体由白变蓝,产生Q3的反应的离子方程式为
为氢气的实验现象是,氢气还原氧化铜固体黑色变化为红色,生成气体中含水蒸气,遇到无水硫酸铜变蓝色,确认含有气体Q3的实验现象是D中固体由黑变红、E中固体由白变蓝,产生Q3的反应的离子方程式为![]() 。
。