题目内容
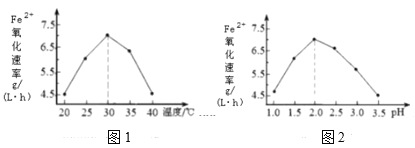
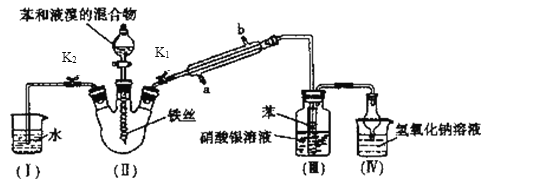
【题目】不同条件下,用O2氧化一定浓度的FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测不合理的是( )
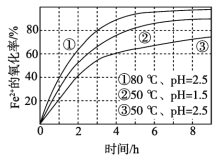
A.Fe2+的氧化率随时间延长而逐渐增大
B.由①和③可知,温度越高,Fe2+氧化速率越快
C.由②和③可知,pH越大,Fe2+氧化速率越快
D.氧化过程的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O
【答案】C
【解析】
A.由图象可知,Fe2+的氧化率随时间延长而逐渐增大,A正确;
B.由①和③可知,当pH相同、温度不同时,温度越高Fe2+的氧化速率越大,B正确;
C.由②和③可知,当温度相同、pH不同时,pH越大,Fe2+的氧化速率越小,C错误;
D.在酸性条件下,Fe2+和氧气、氢离子反应生成Fe3+和H2O,反应的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O,D正确;
故选C。

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目