题目内容
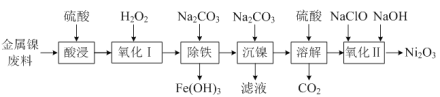
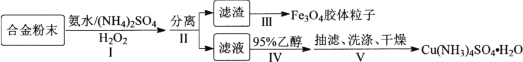
【题目】某学习小组以铝铁铜合金为主要原料制备[Cu(NH3)4]SO4·H2O(一水硫酸四氨合铜)和Fe3O4胶体粒子,具体流程如下:
已知:①Cu(NH3)42+=Cu2++4NH3
②Fe2++2Fe3++8OH![]() Fe3O4↓+4H2O
Fe3O4↓+4H2O
③[Cu(NH3)4]SO4易溶于水,难溶于乙醇。
请回答:
(1) 滤渣的成分为________。
(2) 步骤Ⅰ中生成[Cu(NH3)4]SO4·H2O的离子方程式:________。步骤Ⅰ中加入(NH4)2SO4的作用是作为反应物和________。
(3) 步骤Ⅳ中加入95%乙醇时,缓慢加入的目的是________。
(4) 下列有关叙述正确的是________。
A 步骤Ⅰ缓慢滴加H2O2并不断搅拌,有利于提高H2O2的利用率
B 步骤Ⅳ若改为蒸发浓缩、冷却结晶,得到的一水硫酸四氨合铜晶体会含有较多Cu(OH)2等杂质
C 步骤Ⅳ、Ⅴ用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、吸滤瓶等
D 步骤Ⅴ中洗涤操作为关闭水龙头,加乙醇溶液浸没沉淀,缓慢流干,重复2~3次
(5) 步骤Ⅲ中,从滤渣制备Fe3O4胶体粒子需经过一系列操作。即:滤渣中加过量NaOH溶液搅拌溶解→________→过滤、洗涤、干燥得Fe3O4胶体粒子。
根据下列提供的操作,请在空格处填写正确的操作次序(填写序号)。
①氮气氛围下缓慢滴加NaOH溶液,加热溶液
②过滤、洗涤
③加入过量稀硫酸溶解
④加入适量FeSO4固体,搅拌溶解
⑤测定Fe3+含量
(6) 测定一水硫酸四氨合铜晶体产品的纯度,过程如下:取0.5000 g试样溶于水,滴加3 mol·L1 H2SO4至pH为3~4,加入过量KI固体。以淀粉溶液为指示剂,生成的碘用0.1000 mol·L1 Na2S2O3标准溶液滴定,重复2~3次,平均消耗Na2S2O3标准溶液20.00 mL。。该试样中一水硫酸四氨合铜的纯度为________。
已知:M[Cu(NH3)4SO4·H2O]=246.0 g·mol1; 2Cu2++4I=2CuI+I2,I2+2S2O32-=2I+S4O62-。
【答案】Al(OH)3、Fe(OH)3 Cu+H2O2+2NH3+2![]() =Cu(NH3)42++2H2O或Cu+H2O2+2NH3·H2O+2
=Cu(NH3)42++2H2O或Cu+H2O2+2NH3·H2O+2![]() = Cu(NH3)42++4H2O 抑制NH3·H2O的电离或促进生成Cu(NH3)42+(
= Cu(NH3)42++4H2O 抑制NH3·H2O的电离或促进生成Cu(NH3)42+(![]() 与反应生成的OH成NH3·H2O,控制pH不能太大,以防H2O2在强碱条件下的分解) 有利于得到较大颗粒的晶体 ABC ②③⑤④① 98.40%
与反应生成的OH成NH3·H2O,控制pH不能太大,以防H2O2在强碱条件下的分解) 有利于得到较大颗粒的晶体 ABC ②③⑤④① 98.40%
【解析】
(1)合金粉末进行分离,铝铁应转化为滤渣形式,从所给物质分析,只能是氢氧化铝和氢氧化铁形式,铜转化为[Cu(NH3)4]SO4,利用[Cu(NH3)4]SO4难溶于乙醇,进行分离。
(1)合金粉末溶于氨水和硫酸铵以及过氧化氢的作用下,能进行分离,铁和铝都转化为滤渣,说明滤渣为 Al(OH)3、Fe(OH)3 ;
(2)铜在氨水和硫酸铵和过氧化氢存在反应生成[Cu(NH3)4]SO4,离子方程式为 Cu+H2O2+2NH3+2![]() =Cu(NH3)42++2H2O或Cu+H2O2+2NH3·H2O+2
=Cu(NH3)42++2H2O或Cu+H2O2+2NH3·H2O+2![]() = Cu(NH3)42++4H2O; 硫酸铵不仅提供铵根离子抑制氨水的电离,还可以抑制pH不能太大,以防H2O2在强碱条件下的分解;
= Cu(NH3)42++4H2O; 硫酸铵不仅提供铵根离子抑制氨水的电离,还可以抑制pH不能太大,以防H2O2在强碱条件下的分解;
(3)因为[Cu(NH3)4]SO4在乙醇中的溶解度小,加入95%乙醇有利于得到较大颗粒的晶体;
(4) A.因为过氧化氢能够分解,所以在步骤Ⅰ缓慢滴加H2O2并不断搅拌,有利于提高H2O2的利用率,故正确;B.步骤Ⅳ若改为蒸发浓缩、冷却结晶,蒸发过程中促进反应,Cu(NH3)42+ Cu2++4NH3,氨气逸出,铜离子水解生成氢氧化铜,所以得到的一水硫酸四氨合铜晶体会含有较多Cu(OH)2等杂质,故正确;C.步骤Ⅳ、Ⅴ是进行抽滤和洗涤,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、吸滤瓶等,故正确;D.步骤Ⅴ中洗涤操作为关闭水龙头,加乙醇溶液浸没沉淀,然后进行抽滤,不能缓慢流干,故错误。故选ABC;
(5) 滤渣为氢氧化铝和氢氧化铁的混合物,加过量NaOH溶液搅拌,氢氧化铝溶解生成偏铝酸钠,然后过滤出氢氧化铁沉淀,加入过量的稀硫酸将其溶解生成铁离子,测定铁离子的含量,控制量,加入适量的硫酸亚铁固体,在氮气的氛围下缓慢加入氢氧化钠溶液,加热使其按方程式Fe2++2Fe3++8OH![]() Fe3O4↓+4H2O中的比例进行反应,生成四氧化三铁,再进行过滤、洗涤、干燥得Fe3O4胶体粒子.,故操作顺序为②③⑤④①;
Fe3O4↓+4H2O中的比例进行反应,生成四氧化三铁,再进行过滤、洗涤、干燥得Fe3O4胶体粒子.,故操作顺序为②③⑤④①;
(6)根据反应2Cu2++4I2CuI+I2,I2+2S2O32-2I+S4O62-得关系式为2Cu2+----I2---2S2O32-, Na2S2O3的物质的量为0.1000×0.02=0.002mol则铜离子的物质的量为0.002mol,则Cu(NH3)4SO4·H2O的质量为0.002mol×246.0g/mol=0.492g,质量分数为![]() 。
。

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案