题目内容
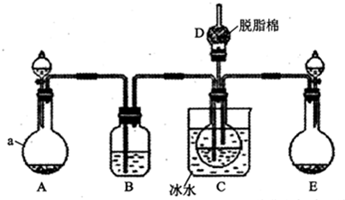
3.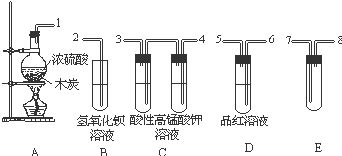 浓H2SO4与炭反应,产物成分可用如图装置来确认:
浓H2SO4与炭反应,产物成分可用如图装置来确认:(1)A 装置中反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(2)B 装置中反应的离子方程式Ba2++2OH-+CO2═BaCO3↓+H2O;
(3)装置 C 的作用是除去SO2,E 中盛放的试剂是无水CuSO4固体;
(4)请用1、2…等标号,写出装置的连接顺序:1-7-8-6-5-4-3-2.
分析 浓H2SO4与炭反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O产物的检验,产物有CO2、SO2、H2O三种,
CO2↑+2SO2↑+2H2O产物的检验,产物有CO2、SO2、H2O三种,
首先根据题目中提供的药品及需要检验的物质,确定每一种产物检验所需试剂,检验SO2用品红溶液,品红褪色;检验CO2用氢氧化钡溶液,变浑浊,但是SO2也可以使氢氧化钡溶液变浑浊,会干扰CO2的检验,故先检验SO2,检验之后再用酸性高锰酸钾溶液除去,还要考虑不同物质检验时是否互相有干扰以及物质检验的先后顺序问题,检验SO2、CO2都会引入水,所以三种物质中最先检验H2O再检验SO2再出去SO2最后检验CO2.
解答 解:(1)浓H2SO4与炭反应方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(2)用氢氧化钡溶液来检验CO2,所以B装置中是CO2与Ba(OH)2的反应,离子方程式为:Ba2++2OH-+CO2═BaCO3↓+H2O
故答案为:Ba2++2OH-+CO2═BaCO3↓+H2O
(3)检验SO2用品红溶液,品红褪色;检验CO2用氢氧化钡溶液,变浑浊,但是SO2也可以使氢氧化钡溶液变浑浊,会干扰CO2的检验,故先检验SO2,检验之后再用酸性高锰酸钾溶液除去,装置 C 的作用是除去SO2;E装置来检验生成的H2O,检验H2O用无水CuSO4固体,CuSO4+5H2O=CuSO4•5H2O,有白色粉末变成蓝色,所以E装置盛放的是无水CuSO4固体.
故答案为:除去SO2、无水CuSO4固体
(4)检验SO2、CO2都会引入水,所以三种物质中最先检验H2O再检验SO2再出去SO2最后检验CO2,注意仪器的连接顺序问题(检验气体或洗气均需长进短出).
故答案为:7-8-6-5-4-3-2.
点评 该题目以浓H2SO4与炭反应为载体,主要考查“气体的检验”等考点的理解,难度不大,但是注意细节问题(SO2、CO2均可使氢氧化钡溶液变浑浊,所以先检验HSO2再除去SO2最后检验CO2)

 阅读快车系列答案
阅读快车系列答案| A. | 它们都是极性键形成的极性分子 | |
| B. | 它们的成键方式都只有σ键 | |
| C. | 可燃冰的存在说明甲烷和水分子间能形成氢键 | |
| D. | 它们的分子空间构型都相同 |
 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )①氧化 ②还原 ③取代 ④加成 ⑤消去 ⑥中和 ⑦缩聚 ⑧酯化.
| A. | ②④⑥⑦⑧ | B. | ⑤④③①⑧ | C. | ①⑤④③⑧ | D. | ②①⑤③⑥ |
| A. | HnX | B. | H(2m-n)X | C. | H(8+n-2m) X | D. | H(8+2m-n) X |
 在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分,当左边充入1molN2,右边充入8gCO和CO2的混合气体,隔板处于如图所示位置(两侧温度相同),则混合气体中CO和CO2的总物质的量为0.25mol,其中CO和CO2的分子数之比为3:1.
在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分,当左边充入1molN2,右边充入8gCO和CO2的混合气体,隔板处于如图所示位置(两侧温度相同),则混合气体中CO和CO2的总物质的量为0.25mol,其中CO和CO2的分子数之比为3:1.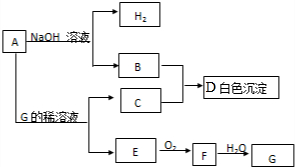
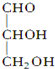

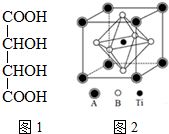 钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.
钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.