题目内容
关于平衡常数,下列说法不正确的是
| A.平衡常数随温度的改变而改变 |
| B.使用催化剂不能改变平衡常数 |
| C.平衡常数不随反应物或生成物浓度的改变而改变 |
| D.增大压强促使平衡向正反应方向进行,则平衡常数增大 |
D
解析试题分析:平衡常数只与温度有关,温度改变,平衡常数一定改变,与反应物、生成物的浓度无关,所以A、C正确;催化剂只改变反应速率,不会改变平衡,所以平衡常数不变,B错误;平衡正向移动,平衡常数增大,D正确;故选D。
考点:本题主要考查平衡常数的定义、影响因素以及应用。

练习册系列答案
相关题目
一定条件下,向密闭容器中充入1 mol N2和3mol H2,发生反应:N2(g) + 3H2(g) 2NH3(g),反应达到平衡后,改变下述条件,再次达到平衡,NH3浓度与原平衡不同的是
2NH3(g),反应达到平衡后,改变下述条件,再次达到平衡,NH3浓度与原平衡不同的是
| A.保持温度和压强不变,充入1 mol NH3(g) |
| B.保持温度和体积不变,充入1 mol Ar(g) |
| C.保持温度和压强不变,充入1 mol N2(g) 和3mol H2 (g) |
| D.保持温度和压强不变,充入1 mol Ar(g) |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)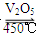 2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是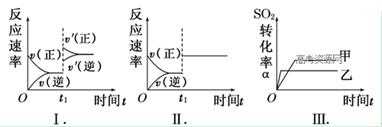
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化剂效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
下列说法正确的是
| A.放热反应一定都是自发的 |
| B.电解池的反应属于自发过程 |
| C.反应能否自发进行与温度有关 |
| D.能自发进行的化学反应,一定是△H>0、△S>0 |
下列有关平衡常数(K、Ka、Kw、Ksp)的说法中错误的是
| A.若各平衡常数(K、Ka、Kw、Ksp)的值发生变化,则平衡一定发生移动 |
| B.若温度升高,则各平衡常数一定增大 |
| C.平衡常数的大小能说明反应(或电离、溶解)进行的程度 |
| D.某一可逆反应的平衡常数越大,表明反应(或电离、溶解)进行的程度越大 |
某温度下,X(g)+Y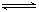 2Z反应达到平衡,在升高温度或减小压强的情况下,平衡均向右移动,则下列有关反应的各种叙述中正确的是
2Z反应达到平衡,在升高温度或减小压强的情况下,平衡均向右移动,则下列有关反应的各种叙述中正确的是
| A.正反应是吸热反应,Z是固体 |
| B.逆反应是放热反应,Y是固体,Z为气体 |
| C.正反应是吸热反应,只有Z不是气体 |
| D.正反应是放热反应,Y和Z均为气体 |
可逆反应2HI(g) H2+I2(g)在密闭容器中装入1molHI气体在一定条件下使它分解,已知有35%发生分解,则容器内混合气体的总物质的量是
H2+I2(g)在密闭容器中装入1molHI气体在一定条件下使它分解,已知有35%发生分解,则容器内混合气体的总物质的量是
| A.1mol | B.0.5mol | C.1.5mol | D.2mol |
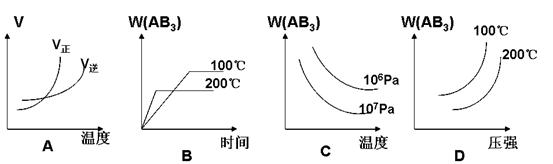
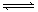 2AB3(g) △H<0(正反应放热),下列图像(其中W为质量分数)不正确的是 ( )
2AB3(g) △H<0(正反应放热),下列图像(其中W为质量分数)不正确的是 ( )