题目内容
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)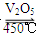 2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是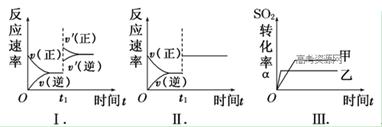
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化剂效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
B
解析试题分析:A、增大反应物的浓度瞬间,正反速率增大,逆反应速率不变,图Ⅰ应是增大压强的原因,故A错误;B、图Ⅱ正正逆反应速率同等程度的增大,为催化剂对反应的影响,故B正确;C、图Ⅲ甲、乙两个平衡状态不同,而加入催化剂,平衡不发生移动,故C错误;D、乙到达平衡时间较短,说明乙的压强大,压强增大则SO2转化率也增大,而图像中甲的SO2转化率反而比乙的大,故D错误。故选B。
考点:考查外界条件对化学反应速率、化学平衡的影响。

练习册系列答案
相关题目
、某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) 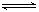 Z(g)+W(s);ΔH>0 下列叙述正确的是
Z(g)+W(s);ΔH>0 下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡状态 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入X,上述反应的ΔH增大 |
下列各组实验中溶液最先变浑浊的是( )
| A.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B.0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度30℃ |
| D.0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
一定温度下反应N2+O2 2NO在密闭容器中进行,下列措施不改变化学反应速率的是
2NO在密闭容器中进行,下列措施不改变化学反应速率的是
| A.缩小体积使压强增大 | B.恒容,充入N2 |
| C.恒容,充入He | D.恒压,充入He |
对于反应C(s)+H2O(g)  CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
A.平衡常数表达式为K=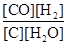 |
| B.增大体系压强,平衡常数K不发生变化 |
| C.升高体系温度,平衡常数K减小 |
| D.增加C(s)的量,平衡正向移动 |
下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B.合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 |
C.反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
D.对于2HI(g) H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
关于平衡常数,下列说法不正确的是
| A.平衡常数随温度的改变而改变 |
| B.使用催化剂不能改变平衡常数 |
| C.平衡常数不随反应物或生成物浓度的改变而改变 |
| D.增大压强促使平衡向正反应方向进行,则平衡常数增大 |
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是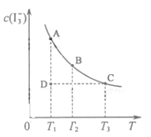
A.反应 I2(aq)+I-(aq) I3-(aq)的ΔH<0 I3-(aq)的ΔH<0 |
B.若温度为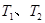 ,反应的平衡常数分别为K1、K2,则K1>K2 ,反应的平衡常数分别为K1、K2,则K1>K2 |
C.若反应进行到状态D时,一定有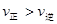 |
| D.状态A与状态B相比,状态A的c(I2)大 |