题目内容
【题目】设![]() 为阿伏伽德罗常数的值,下列说法不正确的是
为阿伏伽德罗常数的值,下列说法不正确的是
A.常温下,1LpH=10的![]() 溶液中所含
溶液中所含![]() 的数目为
的数目为![]() NA
NA
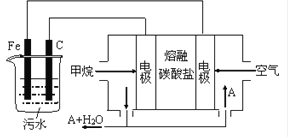
B.氯碱工业中转移2mol电子时,通过阳离子交换膜的![]() 的数目为2NA
的数目为2NA
C.过量的铜与含0.2mol![]() 的浓硝酸反应,转移电子的数目大于0.1NA
的浓硝酸反应,转移电子的数目大于0.1NA
D.室温下向1LpH=1的醋酸溶液中加水稀释,所得溶液中![]() 的数目大于0.1NA
的数目大于0.1NA
【答案】AB
【解析】
A.pH=10的碳酸钠溶液中c(OH-)=10-4mol/L,所以1L该溶液所含氢氧根的物质的量为10-4mol,故A错误;
B.氢氧根为阴离子,不能通过阳离子交换膜,故B错误;
C.若0.2molHNO3全部被铜还原为NO2,则转移0.1mol电子,但是铜和硝酸反应过程中硝酸变稀会生成NO,N的化合价降低3价,所以转移的电子数目大于0.1NA,故C正确;
D.1LpH=1的醋酸溶液中n(H+)=1L×0.1mol/L=0.1mol,加水稀释促进醋酸的电离,从而电离出更多的氢离子,所得溶液中H+的数目大于0.1 NA,故D正确;
故答案为AB。

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目