题目内容
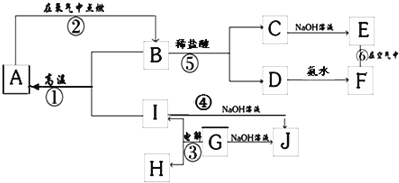
【题目】A~L分别表示中学化学中常见的一种物质,其中A、G为常见的金属单质,K、L为气体,K能使湿润的红色石蕊试纸变蓝,M由两种元素组成,其质量比8:1。
(1)K的电子式为_____
(2)反应②的离子方程式:_____,反应③的离子方程式:_____
(3)反应④的化学方程式:_____,反应⑥的化学方程式_____
(4)已知A和K反应为置换反应,则M的化学式为_____
【答案】![]() Fe3O4+8H+=2Fe3++Fe2++H2O Fe3++3NH3H2O=Fe(OH)3↓+3NH4+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 Al2O3+2NaOH═2NaAlO2+H2O Fe2N
Fe3O4+8H+=2Fe3++Fe2++H2O Fe3++3NH3H2O=Fe(OH)3↓+3NH4+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 Al2O3+2NaOH═2NaAlO2+H2O Fe2N
【解析】
K能使湿润的红色石蕊试纸变蓝,应为NH3,由转化关系可知A为变价金属,则为Fe,可知B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2、F为Fe(OH)3,A和K反应为置换反应,M由两种元素组成,其质量比8:1,则应为Fe2N,L为H2,G为O2,H为Al、I为Al2O3,J为NaAlO2,以此解答该题。
(1)K为氨气,电子式为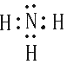 ,故答案为:
,故答案为: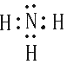 ;
;
(2)反应②为Fe3O4与盐酸的反应,离子方程式为Fe3O4+8H+=2Fe3++Fe2++H2O,反应③为FeCl3与氨水的反应,离子方程式为Fe3++3NH3H2O=Fe(OH)3↓+3NH4+,故答案为:Fe3O4+8H+=2Fe3++Fe2++H2O;Fe3++3NH3H2O=Fe(OH)3↓+3NH4+;
(3)反应④的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,反应⑥的化学方程式为Al2O3+2NaOH═2NaAlO2+H2O,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;Al2O3+2NaOH═2NaAlO2+H2O;
(4)由以上分析可知M为Fe2N,故答案为:Fe2N。