题目内容
【题目】为从粗食盐水中除去Ca2+、Mg2+、SO42-等离子,以制得精盐水。某同学设计如下方案:
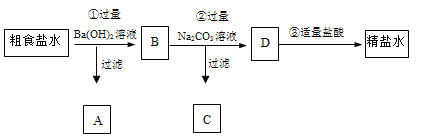
以下说法正确的是( )
A.A中主要有Mg(OH)2和BaSO4,也可能有一些Ca(OH)2
B.②中加入过量Na2CO3溶液的主要目的是为了除去Mg2+、Ca2+
C.D中有CO32-、Cl- 、Na+ 这3种离子
D.③中发生的反应只有2H++CO32-= H2O +CO2↑
【答案】A
【解析】
将粗食盐水加入过量的氢氧化钡,主要除去Mg2+、SO42-,则A中主要有Mg(OH)2和BaSO4沉淀,由于Ca(OH)2溶解度较小,则产物中也可能有一些Ca(OH)2沉淀,B中主要含有Ca2+,Ba2+,OH-,需用过量碳酸钠除去钡离子和钙离子,D中含有Cl-,Na+,CO32-,OH-,,C中为碳酸钡和碳酸钙沉淀,D中加入适量盐酸,除去过量的CO32-,OH-,得到氯化钠溶液。
A. 为从粗食盐水中除去Ca2+、Mg2+、SO42-等离子,加入过量氢氧化钡,Mg2+与OH-反应生成氢氧化镁沉淀,SO42-与Ba2+生成硫酸钡沉淀,Ca(OH)2的溶解度较小,Ca2+与OH-也会生成少量Ca(OH)2沉淀,故A正确;
B. B中含有Ca2+,Ba2+,OH-,中加入过量Na2CO3溶液的主要目的是为了除去Ca2+,Ba2+,故B错误;
C. B中含有Ca2+、Ba2+、OH-,加入过量Na2CO3后,D中含有Cl-、Na+、CO32-、OH-,故C错误;
D. D中加入适量盐酸,除去CO32-、OH-,则③发生的反应有2H++CO32-= H2O +CO2↑,H++OH-= H2O,故D错误;
答案选A。

【题目】(1)葡萄酒中SO2最大使用量为0.25 g·L-1,取300.00 mL葡萄酒,通过适当的方法使 所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定。
①滴定前排气泡时,应选择下图中的________(填序号)。
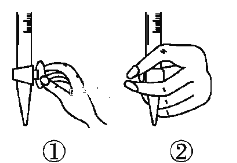
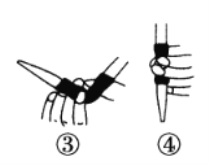
②若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___(填序号)。
①=10 mL ②=40 mL ③<10 mL ④>40 mL。
③上述滴定实验中,可选择___为指示剂,选择该指示剂时如何判断反应到达滴定终点:_____。
④滴定终点读数时俯视刻度线,则测量结果比实际值________(填“偏高”、“偏低”或“无影响”)。
(2)某学生用0.100molL-1的KOH标准溶液滴定未知浓度的盐酸,其操作为:
A.移取20mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准KOH溶液滴定至终点并记下刻度。
实验编号 | KOH溶液的浓度(mol/L) | 滴定完成时,KOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①正确操作步骤的顺序是(用序号字母填写)___________________________
②根据上述数据,可计算出该盐酸的浓度约为______________(保留两位有效数字)。