题目内容
8.可逆反应:2NO2(g)?2N0(g)+O2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO
②单位时间内消耗nmolO2的同时消耗2nmolNO2
③v正(NO2):v正(NO):v正(O2)=2:2:1的状态
④混合气体的密度不再改变的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态.
| A. | ②④⑤ | B. | ②⑤⑥ | C. | ②③④⑥ | D. | ①④⑤⑥ |
分析 化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答 解:2NO2?2NO+O2
①单位时间内生成n mol O2是正反应,同时生成2n mol NO也是正反应,故不能说明达到平衡状态,故错误;
②单位时间内生成n mol O2是正反应,同时生成2n mol NO2是逆反应,且化学反应速率之比等于化学计量数之比,故正逆反应速率相等,故正确;
③化学反应速率之比等于化学计量数之比,故用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态不能作为判断是否达到平衡状态的依据,故错误;
④密度=$\frac{△m}{V}$,总质量不变,体积不变,故混合气体的密度不再改变的状态不能作为判断是否达到平衡状态的依据,故错误;
⑤一氧化氮和氧气为无色气体,二氧化氮为红棕色气体,故混合气体的颜色不再改变的状态可作为判断是否达到化学平衡状态的依据,故正确;
⑥平均相对分子质量=$\frac{总重量}{总物质的量}$,总质量不变,总物质的量会变,故混合气体的平均相对分子质量不再改变的状态可作为判断是否达到化学平衡状态的依据,故正确;
故达到平衡状态的标志是②⑤⑥,
故选B.
点评 本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
相关题目
20.在某溶液中滴加用硝酸酸化的氯化钡溶液,有白色沉淀生成,则该溶液中( )
| A. | 一定含有SO42- | B. | 一定含有Ag+ | ||
| C. | 一定含有SO42-和Ag+ | D. | 可能含有SO42-或Ag+ |


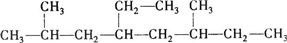 ,那么 1mol该烃完全燃烧需消耗氧气的量为18.5mol.
,那么 1mol该烃完全燃烧需消耗氧气的量为18.5mol.