题目内容
3.某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用.其实验方案如下:
试回答下列问题:
(1)过滤用的器材已有:滤纸、铁架台、铁圈和烧杯,还要补充的玻璃仪器是:玻璃棒、漏斗.
(2)写出下列符号对应物质的化学式:ANaAlO2CCO2DAl(OH)3EFeSO4
(3)反应①的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑;反应②的离子方程式是Fe+2H+=Fe2++H2↑;反应③的离子方程式是Al(OH)3+3H+=Al3++3H2O
途径Ⅱ的方程式是NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3.
(4)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是途径Ⅱ,理由是因为滤液A是NaAlO2和NaOH溶液,按途径I直接向A中加入盐酸得到的AlCl3溶液中含有大量的NaCl杂质,按途径Ⅱ,通入CO2气体,得Al(OH)3沉淀,将Al(OH)3溶解于盐酸中得到的是纯净的AlCl3溶液.所以途径Ⅱ更合理.
(5)如何检验E中的金属阳离子?取少许溶液E与试管中,滴加KSCN溶液,溶液不变红色,再滴加新制氯水,溶液变为红色,说明含有Fe2+,涉及的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-?Fe(SCN)3.
分析 含有铝、铁、铜的合金加入氢氧化钠溶解,只有铝与氢氧化钠反应生成偏铝酸钠和氢气,所以滤渣B为铁和铜,再经稀硫酸反应过滤的滤液为硫酸亚铁,进一步转化成绿矾,滤渣F为铜单质,进一步转化成胆矾;滤液A则为偏铝酸钠溶液,加过量盐酸经途径Ⅰ生成氯化铝溶液,而滤液A通足量气体C经途径Ⅱ生成沉淀D,根据氢氧化铝只溶于强酸强碱,所以气体C为二氧化碳,沉淀D为氢氧化铝,与盐酸反应生成氯化铝溶液.
(1)根据以上分析,该流程需要过滤操作,所以还需的玻璃仪器为玻璃棒、漏斗;
(2)含有铝.铁.铜的合金加入氢氧化钠溶解,只有铝与氢氧化钠反应,滤液A为NaAlO2,在滤液A中通入足量的C气体得到沉淀,为氢氧化铝,所以C为二氧化碳;D为氢氧化铝,滤渣B为铁和铜,再经稀硫酸反应过滤的滤液为硫酸亚铁;
(3)反应①为铝和氢氧化钠溶液反应,反应②为铁和硫酸反应,反应③为氢氧化铝和盐酸反应;途径Ⅱ为偏氯酸钠和二氧化碳和水反应生成氢氧化铝沉淀;
(4)途径Ⅰ会引入氯化钠杂质;而途径Ⅱ能制得纯净的AlCl3溶液;
(5)E为FeSO4溶液,检验Fe2+方法:二价铁易被空气中的氧气氧化成三价铁离子,检验三价铁离子用KSCN溶液.
解答 解:(1)过滤时需要制作过滤器的漏斗、滤纸,固定仪器的铁架台,引流用的玻璃棒,承接滤液的烧杯,所以还需的玻璃仪器为:玻璃棒、漏斗,
故答案为:玻璃棒、漏斗;
(2)含有铝.铁.铜的合金加入氢氧化钠溶解,只有铝与氢氧化钠反应生成偏铝酸钠和氢气,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,所以滤液A为NaAlO2,在NaAlO2溶液中通过过量的二氧化碳气体,发生NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,所以C为CO2,生成的D为氢氧化铝,滤渣B为铁和铜,再经稀硫酸反应过滤的滤液为硫酸亚铁,进一步转化成绿矾,所以E为FeSO4,
故答案为:NaAlO2;CO2;Al(OH)3;FeSO4;
(3)反应①为铝和氢氧化钠溶液反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑,离子反应为:2Al+2OH-+2H2O=2AlO2-+3H2↑,反应②为铁和硫酸反应Fe+H2SO4=FeSO4+H2↑,离子反应为:Fe+2H+=Fe2++H2↑,反应③为氢氧化铝和盐酸反应,离子方程式为Al(OH)3+3H+=Al3++3H2O,途径Ⅱ为偏氯酸钠和二氧化碳和水反应生成氢氧化铝沉淀,NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;Fe+2H+=Fe2++H2↑;Al(OH)3+3H+=Al3++3H2O;NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;
(4)NaAlO2溶液,经途径Ⅰ与足量盐酸反应可生成AlCl3溶液,但溶液中混有NaCl,在NaAlO2溶液中通过过量的二氧化碳气体,发生AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,生成的氢氧化铝再和盐酸反应生成AlCl3,途径Ⅱ得到的AlCl3较纯净,
故答案为:途径Ⅱ;因为滤液A是NaAlO2和NaOH溶液,按途径I直接向A中加入盐酸得到的AlCl3溶液中含有大量的NaCl杂质,按途径Ⅱ,通入CO2气体,得Al(OH)3沉淀,将Al(OH)3溶解于盐酸中得到的是纯净的AlCl3溶液.所以途径Ⅱ更合理;
(5)E为FeSO4溶液,检验Fe2+方法:取少许溶液E与试管中,滴加KSCN溶液,溶液不变红色,再滴加新制氯水,溶液变为红色,说明含有Fe2+,反应为:2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-?Fe(SCN)3,
故答案为:取少许溶液E与试管中,滴加KSCN溶液,溶液不变红色,再滴加新制氯水,溶液变为红色,说明含有Fe2+;2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-?Fe(SCN)3.
点评 本题主要考查了从工业废料中制取纯净物,注意从框图转化中找出有用信息,侧重于学生的分析能力、实验能力的考查,为高考常见题型,注意把握实验的操作原理和步骤,把握相关物质的性质,题目难度中等.

| A. | 1 mol B和3 mol C | |
| B. | 2 mol A、1mol B和1 mol He(不参加反应) | |
| C. | 1 mol B和1 mol C | |
| D. | 2 mol A、3mol B和3 mol C |
| A. | Cu$\stackrel{浓硝酸}{→}$ Cu(NO3)2 | B. | Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 | ||
| C. | Cu$\stackrel{硝酸银溶液}{→}$Cu(NO3)2 | D. | Cu $\stackrel{氧气}{→}$CuO$\stackrel{稀硝酸}{→}$Cu(NO3)2 |
是( )
①单位时间内生成nmolO2的同时生成2nmolNO
②单位时间内消耗nmolO2的同时消耗2nmolNO2
③v正(NO2):v正(NO):v正(O2)=2:2:1的状态
④混合气体的密度不再改变的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态.
| A. | ②④⑤ | B. | ②⑤⑥ | C. | ②③④⑥ | D. | ①④⑤⑥ |
| A. | N溶液无颜色 | |
| B. | M溶液里的两种阳离子为Na+和NH4+ | |
| C. | N溶液滴入BaCl2溶液无明显现象 | |
| D. | M溶液中通入足量CO2有白色沉淀生成 |
| A. | ①③⑦ | B. | ③④⑦ | C. | ③⑦⑧ | D. | ③⑥⑧ |
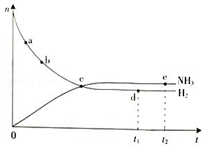 合成氨工业对国民经济和社会发展具有重要的意义.根据已学知识回答下列问题:
合成氨工业对国民经济和社会发展具有重要的意义.根据已学知识回答下列问题: 一学习小组利用如图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液.
一学习小组利用如图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液.