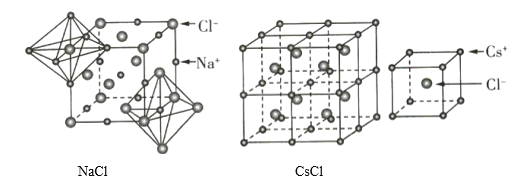
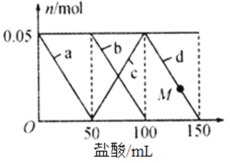
题目内容
【题目】已知某些共价键的键能如表所示,试回答下列问题:℃
共价键 | 键能 | 共价键 | 键能 |
| 436 |
| 467 |
| 243 |
| 945 |
| 413 |
| 431 |
(1)![]() 键的键能为什么比
键的键能为什么比![]() 键的键能大_______?
键的键能大_______?
(2)已知![]() 在
在![]() 时有
时有![]() 的分子分解,而
的分子分解,而![]() 在
在![]() 时可能完全分解为
时可能完全分解为![]() 和
和![]() ,试解释其中的原因_______。
,试解释其中的原因_______。
(3)试解释氮气能在空气中稳定存在的原因_______。
【答案】![]() 原子的半径比
原子的半径比![]() 原子的半径小,故
原子的半径小,故![]() 键的键长比
键的键长比![]() 键的键长短,
键的键长短,![]() 键的键能比
键的键能比![]() 键的键能大
键的键能大 ![]() 键比
键比![]() 键的键能大,故
键的键能大,故![]() 比
比![]() 稳定
稳定 ![]() 分子中存在氮氮叁键,键能大,故结构稳定
分子中存在氮氮叁键,键能大,故结构稳定
【解析】
从原子半径、共价键共用电子对数目出发分析键能的强弱及物质的稳定性。
(1)氢原子的半径比氯原子的半径小,故![]() 键的键长比
键的键长比![]() 的键长短,键长短,不易断裂,键能更大,则
的键长短,键长短,不易断裂,键能更大,则![]() 的键能大;
的键能大;
(2)由题意可知,水比甲烷稳定,则水的键能更大;碳的半径大于氧的半径,故水中化学键键长更短,键能更大,物质更稳定;答案为:![]() 键比
键比![]() 键的键能大,故
键的键能大,故![]() 比
比![]() 稳定;
稳定;
(3)![]() 分子中存在氮氮叁键,键能大,故氮气能在空气中稳定存在;故答案为:
分子中存在氮氮叁键,键能大,故氮气能在空气中稳定存在;故答案为:![]() 分子中存在氮氮叁键,键能大,故结构稳定。
分子中存在氮氮叁键,键能大,故结构稳定。

练习册系列答案
相关题目
【题目】.下表是从实验中测得的不同物质中氧氧键的键长和键能数据:
氧氧键 |
|
|
|
|
键长 | 149 | 128 | 121 | 112 |
键能 |
|
|
|
|
其中![]() 、
、![]() 的值尚未测定,但可根据规律推导
的值尚未测定,但可根据规律推导![]() 、
、![]() 、
、![]() 、
、![]() 的大小顺序是
的大小顺序是![]() ,该规律是( )
,该规律是( )
A.成键时,电子数越多,键能越大
B.键长越短,键能越大
C.成键所用电子数越少,键能越大
D.成键时电子对越偏移,键能越大