��Ŀ����
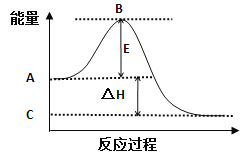
����Ŀ���ϳɰ���ҵ�ĺ��ķ�Ӧ��N2(g)+3H2(g)![]() 2NH3(g)�ķ�Ӧ�����������仯��ͼ��ʾ���ش��������⣺
2NH3(g)�ķ�Ӧ�����������仯��ͼ��ʾ���ش��������⣺
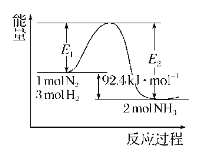
��1����H=______���ڷ�Ӧ��ϵ�м����������Ӧ��������E2�ı仯��______����������������С������������������H (�������С�����䡱)��
��2����500����2��107 Pa�ʹ�����������һ�ܱ������г���0.5 mol N2��1.5 mol H2����ַ�Ӧ�ų�������_______(�<����>������)46.2 kJ������__________________________________��
��3����֪��25����101 kPaʱ��14��CO������ȫȼ�շų�����ΪQ kJ��
��д��COȼ���ȵ��Ȼ�ѧ����ʽ��______________________________________��
���𰸡���1��92.4 kJ/mol ��С ����
��2��< �÷�ӦΪ���淴Ӧ����Ӧ���ת����С��100�����Էų�������С��46.2 kJ
��3��CO(g)+1/2O2(g)![]() 1/2CO2(g) ��H=2Q kJ/mol
1/2CO2(g) ��H=2Q kJ/mol
�����������⿼���˻�ѧ��Ӧ�������ı仯����1���������仯��ͼ��֪��N2(g)+3H2(g)![]() 2NH3(g) ��H= E1 E2=92.4 kJ/mol��ʹ�ô����ı䷴Ӧ;�������ͻ�ܣ���E2��С���Ӵ�����ͬ�ȳ̶ȵĸı����淴Ӧ���ʣ�ƽ�ⲻ�ƶ���������H���䡣
2NH3(g) ��H= E1 E2=92.4 kJ/mol��ʹ�ô����ı䷴Ӧ;�������ͻ�ܣ���E2��С���Ӵ�����ͬ�ȳ̶ȵĸı����淴Ӧ���ʣ�ƽ�ⲻ�ƶ���������H���䡣
��2�����ڸ÷�ӦΪ���淴Ӧ����Ӧ���ת����С��100�������Էų�������С��46.2 kJ��
��3��14��CO������ȫȼ�շų�����Q kJ����1 mol CO������ȫȼ�շų�����Ϊ![]() Q kJ=2Q kJ����COȼ���ȵ��Ȼ�ѧ����ʽΪ��CO(g)+1/2O2(g)
Q kJ=2Q kJ����COȼ���ȵ��Ȼ�ѧ����ʽΪ��CO(g)+1/2O2(g)![]() 1/2CO2(g) ��H=2Q kJ/mol��
1/2CO2(g) ��H=2Q kJ/mol��

����Ŀ��300��ʱ��������X������Y��0.16mol����10L�����ܱ������У�������Ӧ��
X(g)+Y(g)![]() 2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ���� ( )
A. ǰ2min��ƽ����Ӧ����v(X)=2.0��10-2mol/(L��min)
B. �����������䣬�ٳ���0.1 mol X��0.1mol Y���ٴ�ƽ��ʱY��ת���ʲ���
C. ��v��(Y)=2v��(Z)ʱ��˵����Ӧ�ﵽƽ��
D. �÷�Ӧ��250��ʱ��ƽ�ⳣ��С��1.44