��Ŀ����
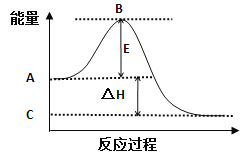
����Ŀ����1��2SO2(g)+O2(g)![]() 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2(g)����Ϊ1 mol SO3(g)�Ħ�H= 99 kJ/mol��
2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2(g)����Ϊ1 mol SO3(g)�Ħ�H= 99 kJ/mol��
��ش��������⣺
��ͼ��A���ʾ�� ��
C���ʾ�� ��
E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ�� (��С����ޡ�)Ӱ�졣
��ͼ�Ц�H = kJ/mol��
��2����������������Ӧ����1 molˮ�������ų�241��8 kJ����(25����101 kPa�²��)
��д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
����1 molˮ����ת��ΪҺ̬ˮ����45kJ����ӦH2(g)��![]() O2(g)
O2(g)![]() H2O( l )�Ħ�H = kJ/mol��������ȼ����Ϊ��H = kJ/mol��
H2O( l )�Ħ�H = kJ/mol��������ȼ����Ϊ��H = kJ/mol��
���𰸡���1������Ӧ��������� ������������� �� ��198
��2��H2 ( g ) +![]() O2 ( g )
O2 ( g )![]() H2O ( g ) ��H ��241.8 kJ/mol
H2O ( g ) ��H ��241.8 kJ/mol
(��2H2 (g) +O2(g)![]() 2H2O(g) ��H ��483.6 kJ/mol)
2H2O(g) ��H ��483.6 kJ/mol)
286.8 286.8
�����������⿼�黯ѧ��Ӧ����������Ӧ�ȵļ��㡢�Ȼ�ѧ����ʽ����д��
��1��������ͼ���֪A�������Ӧ�����������C���ʾ���������������E������ܣ���ܶԷ�Ӧ����Ӱ�죻����Ϊ1 mol SO2(g)����Ϊ1 mol SO3�Ħ�H= 99 kJ��mol1������ͼ���б�ʾ����2 mol���������1 mol���������Է�Ӧ����198 kJ/mol��
��2����������������Ӧ����1 molˮ�������ų�241.8 kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ��H2 (g) +![]() O2 (g)
O2 (g)![]() H2O ( g )��H��241.8 kJ/mol(��2H2 (g) +O2(g)
H2O ( g )��H��241.8 kJ/mol(��2H2 (g) +O2(g)![]() 2H2O(g) ��H��483.6 kJ/mol )������H2 (g) +
2H2O(g) ��H��483.6 kJ/mol )������H2 (g) +![]() O2 (g)
O2 (g)![]() H2O (g)��H��241.8 kJ/mol��H2O(g)
H2O (g)��H��241.8 kJ/mol��H2O(g) ![]() H2O(l) ��H��45 kJ/mol�ã�H2(g)��
H2O(l) ��H��45 kJ/mol�ã�H2(g)��![]() O2(g)
O2(g)![]() H2O(l)�Ħ�H =286.8 kJ/mol����������ȼ����Ϊ��H =286.8 kJ/mol��
H2O(l)�Ħ�H =286.8 kJ/mol����������ȼ����Ϊ��H =286.8 kJ/mol��