题目内容
【题目】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。
![]()
已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为______________。
(2)丙、丁可形成AB2型化合物,其化学式为________。
(3)丙是自然界中形成化合物种类最多的元素,则丙是________(填名称),其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是______________________。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是________(填元素符号),写出这些化合物中任意两种符合以下条件的化学式______________________
(①原子个数比为1∶2;②分子中价电子总数为偶数)。
【答案】第二周期第ⅤA族 CO2 碳 C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O O CO2、N2O、N2O4
CO2↑+4NO2↑+2H2O O CO2、N2O、N2O4
【解析】
设甲的原子序数为n,则根据四种元素的原子序数之和为36可知(n-1)+n+(n+1)+(n+8)=36,解得n=7,即甲为N,由于乙的原子序数等于甲与丁原子序数之和,乙为磷,丁为氧,则丙为碳,据此分析解答。
根据以上分析可知甲为N,乙为P,丙为C,丁为O,则
(1)甲元素是氮元素,在周期表中的位置为第二周期第ⅤA族。
(2)丙、丁可形成AB2型化合物,该化合物是二氧化碳,其化学式为CO2。
(3)丙是自然界中形成化合物种类最多的元素,则丙是碳,其单质与甲元素的最高价氧化物对应水化物的浓溶液,即浓硝酸共热时反应的化学方程式是C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O。
CO2↑+4NO2↑+2H2O。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是O,氧与碳、氮、磷形成的原子个数比为1∶2的化合物有CO2、NO2、N2O、N2O4,其中NO2的价电子总数为奇数,不符合题意。

【题目】(1)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2。反应能够自发进行,则反应的ΔH___0(填“>”“<”或“=”)。
2CO2+N2。反应能够自发进行,则反应的ΔH___0(填“>”“<”或“=”)。
(2)已知:反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。不同温度时K1、K2的值如下表:
FeO(s)+H2(g)的平衡常数为K2。不同温度时K1、K2的值如下表:
温度/K | K1 | K2 |
973 | 1.47 | 2.38 |
1 173 | 2.15 | 1.67 |
根据表中数据,计算反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的K。
CO(g)+H2O(g)的K。
①平衡常数的表达式K1=___;
②温度为973K时:K=___;(结果保留小数点后2位)
③反应CO2(g)+H2(g)![]() CO(g)+H2O(g)是__(填“吸热”或“放热”)反应。
CO(g)+H2O(g)是__(填“吸热”或“放热”)反应。
(3)已知在温度为T时,CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1mol·L-1,c始(H2O)=1mol·L-1,某时刻经测定CO的转化率为10%,则该反应___(填“已经”或“没有”)达到平衡,原因是__;此时刻v正__(填“>”或“<”)v逆。
CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1mol·L-1,c始(H2O)=1mol·L-1,某时刻经测定CO的转化率为10%,则该反应___(填“已经”或“没有”)达到平衡,原因是__;此时刻v正__(填“>”或“<”)v逆。
【题目】以镍废料(主要成分为镍铁合金,含少量铜)为原料,生产NiO的部分工艺流程如下:
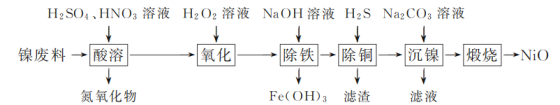
已知:下表列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.3 | 9.9 | 9.2 |
(1) “酸溶”时Ni转化为NiSO4,该过程中温度控制在70~80 ℃的原因是________。
(2) “氧化”时,Fe2+参加反应的离子方程式为________。
(3) “除铁”时需控制溶液的pH范围为________。
(4) “滤渣”的主要成分为________(填化学式)。
(5) “沉镍”时得到碱式碳酸镍[用xNiCO3·yNi(OH)2表示]沉淀。
①在隔绝空气条件下,“煅烧”碱式碳酸镍得到NiO,该反应的化学方程式为________。
②“沉镍”时,溶液pH增大,碱式碳酸镍中Ni元素含量会增加,原因是________。


