题目内容
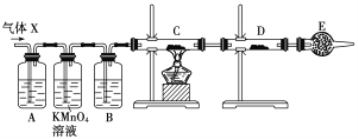
【题目】如图所示装置可用来制取和观察氢氧化亚铁在空气中被氧化时颜色的变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。
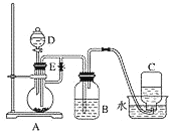
(1)B中盛一定量的氢氧化钠溶液,A中应预先加入的试剂是________,A中反应的离子方程式是_________。
(2)实验开始时就先将止水夹E________(填“打开”或“关闭”),C中收集到气体的主要成分是________。
(3)简述生成氢氧化亚铁的操作过程:__________________。
(4)拔去装置B中的橡皮塞,使空气进入,有关反应的化学方程式是_____________。
【答案】铁屑 Fe+2H+=Fe2++H2↑ 打开 氢气 关闭止水夹E,使硫酸亚铁溶液压入B瓶中进行反应 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
(1)A中应预先盛放固态反应物,铁和稀硫酸发生氧化还原反应生成硫酸亚铁和氢气;
(2)实验开始时,应先打开活塞,使生成的氢气充满整套实验装置中而排出空气,防止氢氧化亚铁被氧化;C中的气体的主要成分为铁和稀硫酸反应生成的氢气;
(3)关闭活塞时,在气体压强的作用下,A中溶液进入B装置中,A中溶液含有硫酸亚铁,可能含有硫酸,硫酸和硫酸亚铁都和氢氧化钠溶液反应;
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀。
(1)A中应预先盛放固态反应物铁屑,铁和稀硫酸反应生成硫酸亚铁和氢气,离子反应方程式为:Fe+2H+=Fe2++H2↑;
(2)实验开始时,应先打开活塞,使生成的氢气进入整套实验装置中而排出空气,防止氢氧化亚铁被氧化;氢气不和水反应,所以C中收集的氢气主要是铁和稀硫酸反应生成的氢气;
(3)关闭活塞时,在气体压强的作用下,A中溶液进入B装置中,A中溶液含有硫酸亚铁,硫酸亚铁都和氢氧化钠溶液反应,因此B中产生白色沉淀氢氧化亚铁;
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以看到的现象是:白色沉淀先转化为灰绿色最后转化为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】下列表格中的各种情况,可以用右图的曲线表示的是 ( )
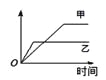
反 应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量的氨,在同一容器中 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
C | 在体积可变的恒压容器中,体积比1︰3的N2、H2, | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2 molSO2和1 molO2,在相同温度下2SO2+ O2 | SO3物质的量 | 2个大气压 | 10个大气压 |
A. AB. BC. CD. D