جâؤ؟ؤعبف
،¾جâؤ؟،؟ؤ³آء؛د½ًضذ؛¬سذشھثطآء،¢أ¾،¢ح،¢¹è£¬خھءث²â¶¨¸أ؛د½ًضذآءµؤ؛¬ء؟£¬ةè¼ئءثبçدآتµر飬اë»ط´ًسذ¹طختجâ£؛
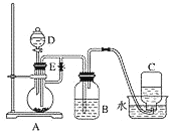
(1)³ئب،رùئ·a g(¾«ب·µ½0.1 g)£¬³ئء؟ت±ح¨³£ت¹سأµؤض÷زھزائ÷µؤأû³ئتا_____،£
(2)½«رùئ·بـ½âسع¹ء؟µؤد،رخثل£¬¹آث²¢د´µسآثشü،£آثز؛ضذض÷زھ؛¬سذ________£¬آثشüخھ________£¬بـ½â،¢¹آثسأµ½µؤ²£ء§زائ÷تا________،£
(3)دٍآثز؛ضذ¼س¹ء؟µؤاâرُ»¯ؤئبـز؛£¬¹آث²¢د´µسآثشü،£سذ¹طµؤہë×س·½³جت½تا________________________________________________________________،£
(4)دٍ²½ضè(3)µؤآثز؛ضذح¨بë×مء؟µؤ¶رُ»¯ج¼ئّجه£¬¹آث²¢د´µسآثشü،£سذ¹طµؤہë×س·½³جت½تا______________________________________________________________،£
(5)½«²½ضè(4)ضذثùµأµؤآثشü؛و¸ة²¢×ئةصضء؛مضط،¢ہنب´؛َ³ئء؟£¬ئنضتء؟خھb g،£سذ¹ط·´س¦µؤ»¯ر§·½³جت½تا
_______________________________________________________________________£¬شرùئ·ضذآءµؤضتء؟·ضتتا________،£
،¾´ً°¸،؟حذإججىئ½HCl،¢MgCl2،¢AlCl3Cu،¢Siةص±،¢²£ء§°ô،¢آ©¶·Mg2£«£«2OH£===Mg(OH)2،،¢Al3£«£«4OH£===AlO2-£«2H2OOH££«CO2===HCO3-،¢AlO£«CO2£«2H2O===Al(OH)3،£«HCO3-)2Al(OH)3![]() Al2O3£«3H2O
Al2O3£«3H2O![]()
،¾½âخِ،؟
£¨1£©ت¹سأحذإججىئ½³ئب،رùئ·ضتء؟£»£¨2£©آءسëرخثلس¦ةْ³ةآب»¯آء،¢Mgسëرخثل·´س¦ةْ³ةآب»¯أ¾£¬µ¥ضت¹è؛حح²»ؤـ¹»؛حد،رخثل·¢ةْ·´س¦£¬ءôشعءثآثشüضذ£»بـ½â،¢¹آث¹³جذèزھزائ÷سذ£؛ةص±،¢آ©¶·،¢²£ء§°ô£»£¨3£©ت£سàµؤرخثلسëاâرُ»¯ؤئ·´س¦ةْ³ةآب»¯ؤئسëث®£¬آب»¯أ¾سëاâرُ»¯ؤئ·´س¦ةْ³ةاâرُ»¯أ¾³ءµيسëآب»¯ؤئ£¬آب»¯آءسë¹ء؟µؤاâرُ»¯ؤئ·´س¦ةْ³ةئ«آءثلؤئسëآب»¯ؤئ£»£¨4£©¹ء؟¶رُ»¯ج¼سëئ«آءثلؤئبفز×·´س¦ةْ³ةاâرُ»¯آء³ءµيسëج¼ثلاâؤئ£»£¨5£©ثùµأ³ءµيخھاâرُ»¯آء£¬¼سبب·ض½âµأµ½رُ»¯آءسëث®£»رُ»¯آءضذAlشھثطضتء؟¼´خھ؛د½ًضذAlµؤضتء؟£¬½ّ¶ّ¼ئثمAlµؤضتء؟·ضت£»
(1)³ئب،a gرùئ·ت¹سأµؤض÷زھزائ÷خھحذإججىئ½،£(2)؛د½ًضذAl،¢Mg؟ةسëرخثل·´س¦ةْ³ةAlCl3،¢MgCl2؛حH2£¬¶ّCu،¢Si²»بـسعرخثل£¬¹ترùئ·بـسعرخثل؛َ¹آث؟ةµأCu،¢Si£¬آثز؛ضذض÷زھ؛¬HCl،¢AlCl3؛حMgCl2،£(3)دٍ(2)µؤآثز؛ضذ¼س¹ء؟NaOHبـز؛£¬·¢ةْµؤ·´س¦خھMg2£«£«2OH£===Mg(OH)2،،¢Al3£«£«4OH£===AlO£«2H2O£¬¹آث؛َآثز؛ضذ؛¬AlO،¢OH£،£(4)دٍ؛¬AlO،¢OH£µؤآثز؛ضذح¨بë×مء؟CO2£¬·¢ةْµؤ·´س¦خھOH££«CO2=== HCO،¢AlO£«CO2£«2H2O===Al(OH)3،£«HCO£¬¹آث؟ةµأAl(OH)3،£(5)ثùµأb g¹ججهخھAl2O3£¬¹ت؛د½ًضذ؛¬Alµؤضتء؟·ضتخھ![]() ،ء100%£½
،ء100%£½![]() %،£
%،£

 جىجىدٍةدز»±¾؛أ¾يدµءذ´ً°¸
جىجىدٍةدز»±¾؛أ¾يدµءذ´ً°¸ ذ،ر§ةْ10·ضضسس¦سأجâدµءذ´ً°¸
ذ،ر§ةْ10·ضضسس¦سأجâدµءذ´ً°¸،¾جâؤ؟،؟دآءذ¶شةْجْئ¬ذâت´¶ش±بتµرéµؤ·ضخِصب·µؤتا£¨ £©
ذٍ؛إ | ¢ظ | ¢ع | ¢غ |
تµرé |
|
|
|
دضدَ | 8ذ،ت±خ´¹غ²ى µ½أ÷دشذâت´ | 8ذ،ت±خ´¹غ²ى µ½أ÷دشذâت´ | 1ذ،ت±¹غ²ى µ½أ÷دشذâت´ |
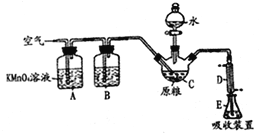
A.¶ش±بتµرé¢ظ¢ع¢غ£¬ثµأ÷±½ؤـ¸ô¾ّO2
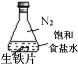
B.تµرé¢ظضذ£¬ةْجْئ¬خ´¼ûأ÷دشذâت´µؤض÷زھشزٍتاب±ةظO2
C.تµرé¢عضذ£¬NaClبـز؛ضذبـ½âµؤO2²»×مزشت¹ةْجْئ¬أ÷دشذâت´
D.تµرé¢غضذ£¬تôسعجْµؤخüرُ¸¯ت´£¬¸؛¼«·´س¦£؛O2+4e-+2H2O=4OH-
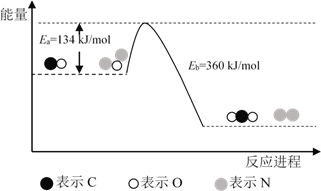
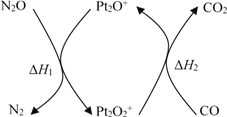
،¾جâؤ؟،؟؟خ±¾ہï½éةـµؤ؛د³ة°±¼¼تُ½ذ¹²®·¨£¬تاµآ¹ْإµ±´¶û»¯ر§½±»ٌµأصك¹²®·¢أ÷µؤ،£ئن؛د³ةشہيخھ£؛N2(g) + 3H2(g) ![]() 2NH3(g) ،÷H<0£¬،÷S <0،£
2NH3(g) ،÷H<0£¬،÷S <0،£
£¨1£©دآءذ¹طسع¹¤زµ؛د³ة°±µؤثµ·¨²»صب·µؤتا_______
A£®زٍخھ،÷H<0£¬ثùزش¸أ·´س¦ز»¶¨ؤـ×ش·¢½ّذذ
B£®زٍخھ،÷S<0£¬ثùزش¸أ·´س¦ز»¶¨²»ؤـ×ش·¢½ّذذ
C£®شع¸كخآدآ½ّذذتاخھءثجل¸ك·´س¦خïµؤ×ھ»¯آت
D£®ت¹سأ´ك»¯¼ء¼س؟ى·´س¦ثظآتتازٍخھ´ك»¯¼ء½µµحءث·´س¦µؤ،÷H
£¨2£©شع؛مخآ؛مبفأـ±صبفئ÷ضذ½ّذذ؛د³ة°±µؤ·´س¦£¬دآءذؤـثµأ÷¸أ·´س¦زر´ïµ½ئ½؛â×´ج¬µؤتا_______
a.بفئ÷ؤعN2،¢H2،¢NH3µؤإ¨¶بض®±بخھ1£؛3£؛2 b.vص(N2)= vؤو(H2)
c.بفئ÷ؤعر¹ا؟±£³ض²»±ن d.؛دئّجهµؤأـ¶ب±£³ض²»±ن
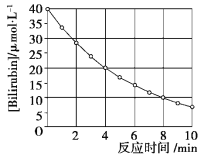
£¨3£©ؤ³؟ئرذذ،×éرذ¾؟£؛شعئنثûجُ¼²»±نµؤاé؟ِدآ£¬¸ؤ±نئًت¼خïاâئّµؤخïضتµؤء؟¶ش¹¤زµ؛د³ة°±·´س¦µؤس°دى،£تµرé½ل¹ûبçح¼ثùت¾£¨ح¼ضذT±يت¾خآ¶ب£¬n±يت¾H2خïضتµؤء؟£©،£

¢ظح¼دَضذT2؛حT1µؤ¹طدµتا£؛T2 __________T1£¨جî،°>£¬<»ٍ=،±£¬دآح¬£©
¢عa،¢b،¢c،¢dثؤµمثù´¦µؤئ½؛â×´ج¬ضذ£¬·´س¦خïN2 µؤ×ھ»¯آت×î¸كµؤتا______£¨جî×ضؤ¸£©،£
£¨4£©؛مخآدآ£¬حùز»¸ِ4Lµؤأـ±صبفئ÷ضذ³نبë5.2mol H2؛ح2mol N2£¬·´س¦¹³جضذ¶شNH3µؤإ¨¶ب½ّذذ¼ى²â£¬µأµ½µؤت¾فبçدآ±يثùت¾£؛
ت±¼ن/min | 5 | 10 | 15 | 20 | 25 | 30 |
c(NH3)/mol،¤L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
¢ظ´ثجُ¼دآ¸أ·´س¦µؤ»¯ر§ئ½؛â³£تK=___________،£
¢عبôخ¬³ضبفئ÷جه»²»±ن£¬خآ¶ب²»±ن£¬حùشئ½؛âجهدµضذ¼سبëH2،¢N2؛حNH3¸÷4mol£¬»¯ر§ئ½؛⽫دٍ_______·´س¦·½دٍزئ¶¯£¨جî،°ص،±»ٍ،°ؤو،±£©،£
¢غN2(g)+3H2(g) ![]() 2NH3(g)،÷H= -92kJ/mol،£شع؛مخآ؛مبفµؤأـ±صبفئ÷ضذ³نبë1mol N2؛حز»¶¨ء؟µؤH2·¢ةْ·´س¦،£´ïµ½ئ½؛â؛َ£¬²âµأ·´س¦·إ³ِµؤببء؟خھ18.4 kJ£¬»ى؛دئّجهµؤخïضتµؤء؟خھ3.6 mol£¬بفئ÷ؤعµؤر¹ا؟±نخھشہ´µؤ90£¥£¬شٍئًت¼ت±³نبëµؤH2µؤخïضتµؤء؟خھ______mol،£
2NH3(g)،÷H= -92kJ/mol،£شع؛مخآ؛مبفµؤأـ±صبفئ÷ضذ³نبë1mol N2؛حز»¶¨ء؟µؤH2·¢ةْ·´س¦،£´ïµ½ئ½؛â؛َ£¬²âµأ·´س¦·إ³ِµؤببء؟خھ18.4 kJ£¬»ى؛دئّجهµؤخïضتµؤء؟خھ3.6 mol£¬بفئ÷ؤعµؤر¹ا؟±نخھشہ´µؤ90£¥£¬شٍئًت¼ت±³نبëµؤH2µؤخïضتµؤء؟خھ______mol،£
£¨5£©زرضھ£؛N2(g)+3H2(g) ![]() 2NH3(g)،÷H= -92kJ/mol
2NH3(g)،÷H= -92kJ/mol
N2(g)+O2(g)£½2NO(g) ¦¤H= +181kJ/mol
2H2(g)+O2(g)£½2H2O(g) ¦¤H= -484kJ/mol
ذ´³ِ°±ئّ´ك»¯رُ»¯ةْ³ةNO؛حث®صôئّµؤبب»¯ر§·½³جت½_________،£