题目内容
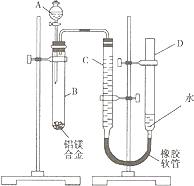
【题目】请根据化学反应与热能的有关知识,填写下列空白:
I. (1)下列ΔH表示物质燃烧热的是________;表示反应中和热ΔH=-57.3 kJ·mol-1的是________(填“ΔH1”“ΔH2”和“ΔH3”等)。
A.C(s)+![]() O2(g)===CO(g) ΔH1
O2(g)===CO(g) ΔH1
B.2H2(g)+O2(g)===2H2O(l) ΔH2
C.C(s)+O2(g)===CO2(g) ΔH3
D.![]() Ba(OH)2(aq)+
Ba(OH)2(aq)+![]() H2SO4(aq)===
H2SO4(aq)===![]() BaSO4(s)+H2O(l) ΔH4
BaSO4(s)+H2O(l) ΔH4
E.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH5
F.2NaOH(aq)+H2SO4(aq)===Na2SO4(aq)+2H2O(l) ΔH6
(2)化学反应的能量变化(ΔH)与反应物和生成物的键能有关(键能可以简单理解为断开1 mol化学键时所需吸收的能量),下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能(kJ·mol-1) | a | 360 | 500 | 434 |
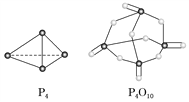
已知白磷(P4)的燃烧热为2 378 kJ·mol-1,白磷完全燃烧的产物(P4O10)的结构如上图所示,则上表中a=________(保留到整数)。
II.已知2mol氢气燃烧生成液态水时放出572KJ热量,反应的热化学方程式是2H2(g)+O2(g)=2H2O(l) △H=-572KJ·mol-1。
(3)该反应生成物的能量总和______(填“大于”“小于”或“等于”)反应物的能量总和。
(4)若2mol氢气完全燃烧生成水蒸气,则放出的热量_______(填“>”“<”或“=”)572KJ。
III.(5)已知16g固体硫完全燃烧时放出148.4KJ的热量,写出表示硫的燃烧热的热化学方程式:____________________________________。
(6)如图所示是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,

请写出NO2和CO反应的热化学方程式:_______________________________。
【答案】 ΔH3 ΔH5 196 小于 < S(s)+O2(g)=SO2(g) △H=-296.8kJ·mol-1 NO2(g)+CO(g)===CO2(g)+NO(g) ΔH=-234 kJ/mol
【解析】I.考查中和热和燃烧热的定义、反应热的计算,(1)根据燃烧热的定义:1mol可燃气体完全燃烧生成稳定的氧化物放出的热量,即属于燃烧热的是△H3;根据中和热的定义:酸与碱反应生成1mol水时放出的热量,即属于中和热的是△H5;(2)根据△H等于反应物键能总和-生成物键能总和,△H=(6×a+5×500-12×360-4×434)=-2378kJ·mol-1,解得a=196kJ·mol-1;II.考查化学能与热能的转化,(3)因为△H<0,说明此反应是放热反应,即反应物的总能量大于生成物的总能量,即反应生成物的总能量小于反应物的能量总和;(4)液态水转化成水蒸气需要吸收热量,因此2mol氢气完全燃烧生辰水蒸气,放出的热量<572kJ;III.考查热化学反应方程式的书写,(5)1molS完全燃烧放出的热量是![]() kJ=296.8kJ,因此硫燃烧热的热化学方程式为 S(s)+O2(g)=SO2(g) △H=-296.8kJ·mol-1; (6)NO2和CO反应的化学方程式为:NO2+CO=CO2+NO,根据能量与过程的图像,则热化学反应方程式为NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234 kJ·mol-1。
kJ=296.8kJ,因此硫燃烧热的热化学方程式为 S(s)+O2(g)=SO2(g) △H=-296.8kJ·mol-1; (6)NO2和CO反应的化学方程式为:NO2+CO=CO2+NO,根据能量与过程的图像,则热化学反应方程式为NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234 kJ·mol-1。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案【题目】X、Y、Z、W和N均是由短周期元素组成的五种化合物.已知五种化合物水溶液的焰色反应均呈黄色,Y、Z和N均由三种元素组成.请根据题目要求回答下列问题.
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有(填序号).
A.离子键
B.极性共价键
C.非极性共价键
D.氢键
(2)写出X与二氧化碳反应的化学方程式 .
(3)下表为Y与Z实验的部分内容:
序号 | 主要实验步骤及实验现象 |
① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
写出Y与稀硫酸反应的离子方程式 .
(4)写出含0.1mol Z的溶液与20mL 5molL﹣1的盐酸反应的离子反应式 . 实验③加热蒸发、灼烧得到的最终产物主要是 .
(5)化合物W和N可以相互转化:W ![]() N.若有W和NxH2O的混合物6.52g,加热到完全反应后,气体产物通过浓硫酸增重1.71g,剩余气体通过碱石灰增重1.10g,则混合物中W的质量为 , NxH2O的化学式为 .
N.若有W和NxH2O的混合物6.52g,加热到完全反应后,气体产物通过浓硫酸增重1.71g,剩余气体通过碱石灰增重1.10g,则混合物中W的质量为 , NxH2O的化学式为 .
【题目】(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成1mo1NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:_____________________________;
(2)若已知下列数据:
化学键 | H-H | N≡N |
键能/kJmol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能______kJmol-1
(3)已知100ml lmol/L的氢氧化钠溶液与适量硫酸溶液完全反应放出5.73kJ的热量,请写出表示中和热的热化学方程式________________________________;
(4)已知1克氢气完全燃烧生成液态水时放出akJ的热量,请写出表示氢气燃烧热的热化学方程式____________________________________________。