题目内容
7.某元素的原子结构示意图为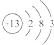 ,下列关于该元素的说法中,错误的是( )
,下列关于该元素的说法中,错误的是( )| A. | 它的阳离子带3个单位正电荷 | B. | 它是一种金属元素 | ||
| C. | 它的阳离子有10个质子 | D. | 其原子核外有13个电子 |
分析 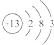 原子序数为13,最外层有3个电子,属于金属元素,失去最外层3个电子容易形成阳离子,据此解答即可.
原子序数为13,最外层有3个电子,属于金属元素,失去最外层3个电子容易形成阳离子,据此解答即可.
解答 解:A、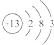 最外层有3个电子,失去最外层3个电子容易形成带3个单位正电荷的阳离子,故A正确;
最外层有3个电子,失去最外层3个电子容易形成带3个单位正电荷的阳离子,故A正确;
B、此微粒的原子序数为13,是铝元素,属于金属元素,故B正确;
C、形成离子只是核外电子数改变,质子数不变,故C错误;
D、Al原子核外电子数=质子数=13,故D正确,
故选C.
点评 本题主要考查的是对微粒结构示意图的认识与理解,掌握质子数等于原子序数、核外电子数与质子数的关系确定阴阳离子,是解决本题的关键,难度不大.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
12.1mol乙醇与一定量的钠刚好完全反应后,溶液增加的质量( )
| A. | 11g | B. | 17g | C. | 44g | D. | 22g |
18.下列各组原子序数所表示的两种元素,能形成AB2型共价化合物的是( )
| A. | 6和8 | B. | 1和7 | C. | 11和16 | D. | 12和17 |
2.下列关于有机物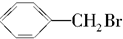 的说法不正确的是( )
的说法不正确的是( )
 的说法不正确的是( )
的说法不正确的是( )| A. | 所有的碳原子在同一个平面上 | |
| B. | 能够发生加成反应 | |
| C. | 不能发生消去反应 | |
| D. | 水解生成的有机物可与NaOH溶液反应 |
12.下列对化合物M、N的叙述正确的是( )


| A. | M的分子式为C12H9O3 | |
| B. | 1mol M在最多能与6molH2发生加成反应 | |
| C. | M与N可用试剂组合:溴水、NaOH溶液鉴别 | |
| D. | M与N可用试剂组合:FeCl3溶液、稀H2SO4鉴别 |
19.新制氯水与久置氯水相比较,下列说法错误的是( )
| A. | 颜色不同 | B. | 都能使滴有酚酞的NaOH溶液褪色 | ||
| C. | 都能使有色布条褪色 | D. | 加AgNO3溶液都能生成白色沉淀 |
16.咖啡酸具有止血功效,存在于多种中药中,其结构简式如图:则下列有关说法正确的是( )
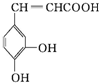

| A. | 该物质中苯环上一氯代物有2种 | |
| B. | 该分子结构中含有两种官能团 | |
| C. | 既能发生取代反应,也能发生加成反应 | |
| D. | 所有碳原子不可能都在同一个平面上 |
