题目内容
16. 某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了如下实验装置,请回答下列问题:
某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了如下实验装置,请回答下列问题:(1)A试管中发生反应的离子方程式2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2↑+H2O.
(2)B试管中的现象是白色沉淀.
(3)该实验设计不严密,请你改正在A和B之间连一个盛有饱和NaHCO3溶液的洗气瓶.
分析 将CH3COOH与Na2CO3发生反应:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,说明酸性CH3COOH>H2CO3;产生的CO2气体通入苯酚钠溶液发生反应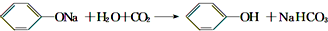 ,说明酸性H2CO3>
,说明酸性H2CO3>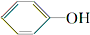 ,据此回答.
,据此回答.
解答 解:将CH3COOH与Na2CO3发生反应:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,说明酸性CH3COOH>H2CO3;产生的CO2气体通入苯酚钠溶液发生反应: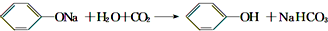 说明酸性H2CO3>
说明酸性H2CO3> ,
,
(1)将CH3COOH与Na2CO3反应生成醋酸钠、水和二氧化碳气体,反应的离子方程式为2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2↑+H2O,
故答案为:2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2↑+H2O;
(2)产生的CO2气体通入苯酚钠溶液发生反应: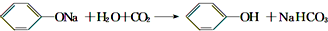 ,苯酚难溶于水,会出现浑浊,生成白色沉淀,
,苯酚难溶于水,会出现浑浊,生成白色沉淀,
故答案为:白色沉淀;
(3)由于醋酸易挥发,则与苯酚钠反应的不一定为二氧化碳,应在A和B之间连一个盛有饱和NaHCO3溶液的洗气瓶,通过饱和碳酸氢钠溶液,除去醋酸,
故答案为:在A和B之间连一个盛有饱和NaHCO3溶液的洗气瓶.
点评 本题考查了探究顺序强弱实验,明确物质的性质是解本题关键,结合强酸制取弱酸实验原理来分析解答,注意:醋酸有挥发性,导致制取的二氧化碳中含有醋酸,干扰实验,为易错点.

练习册系列答案
相关题目
6.下列物质属于等电子体一组的是( )
| A. | CH3Cl和NH4+ | B. | B3H6N3和C6H6 | C. | CO2、NO2 | D. | H2O和CH4 |
7.下列说法中不正确的是( )
| A. | 冰醋酸、酒精、氨气、苯等均是非电解质 | |
| B. | 石油经分馏得到的各种馏分仍然是混合物 | |
| C. | 胶体区别于其他分散系的本质特征是分散质粒子的直径不同 | |
| D. | 玻璃、水泥和陶瓷的主要成分都属于硅酸盐 |
4.近年来流行喝苹果醋.苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等作用的保健食品.苹果酸(α羟基丁二酸)是这种饮料的主要酸性物质,其结构如图所示: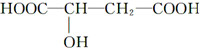
下列相关说法正确的是( )
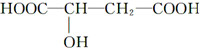
下列相关说法正确的是( )
| A. | 1mol苹果酸在一定条件下能与足量钠反应生成3mol氢气 | |
| B. | 苹果酸在一定条件下能催化氧化生成醛 | |
| C. | 苹果酸在一定条件下能发生加聚反应生成高分子化合物 | |
| D. | 1 mol苹果酸与NaHCO3溶液反应最多消耗2 mol NaHCO3 |
11.分子式为:C7H8O3N2的有机物中符合:氨基与硝基直接连在苯环上并呈对位的同分异构体数有( )
| A. | 12种 | B. | 10种 | C. | 6种 | D. | 4种 |
1.下列实验装置图完全正确的是( )
| A. | 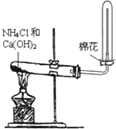 实验室制取并收集氨气 | B. | 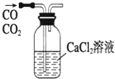 除去CO中混有的CO2 | ||
| C. | 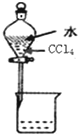 分离水和CCl4的混合物 | D. | 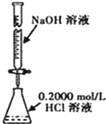 酸碱中和滴定 |
8.将100mL某未知浓度的AlCl3溶液分别加到600mL 0.1mol•L-1的NaOH溶液或600mL 0.3mol•L-1的NaOH溶液中,均能得到1.56g Al(OH)3沉淀.则此AlCl3溶液的浓度可能是( )
| A. | 1 mol•L-1 | B. | 0.5 mol•L-1 | C. | 0.6 mol•L-1 | D. | 0.4 mol•L-1 |
5.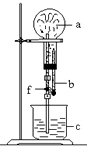 在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶.则a和b分别是( )
在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶.则a和b分别是( )
 在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶.则a和b分别是( )
在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶.则a和b分别是( )| a(干燥气体) | b(液体) | |
| A | NO | NaOH溶液 |
| B | Cl2 | 饱和NaCl溶液 |
| C | CO2 | KOH溶液 |
| D | NO2 | 水溶液 |
| A. | A | B. | B | C. | C | D. | D |
8.下列物质中,属于酯类的是( )
| A. | 甘油 | B. | 汽油 | C. | 润滑油 | D. | 植物油 |