题目内容
8.分类法在化学学科的发展中起到了非常重要的作用.下列分类标准不合理的是( )①根据组成元素将氧化物分成酸性氧化物和碱性氧化物
②根据在水溶液里是否完全电离将电解质分为强电解质和弱电解质
③根据是否有丁达尔现象将分散系分为溶液、胶体和浊液
④根据水溶液是否能导电将化合物分为电解质和非电解质.
| A. | .②③ | B. | .②④ | C. | ①②③ | D. | .①③④ |
分析 ①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物;
②电解质在水溶液中完全电离,而弱电解质电离不完全;
③根据分散系分散质微粒大小将分散系分为溶液、胶体和浊液;
④根据水溶液或是熔融态是否能够导电将化合物分为电解质和非电解质.
解答 解:①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物,不是组成元素,故①错误;
②电解质在水溶液中完全电离,而弱电解质电离不完全,根据电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质,故②正确;
③根据分散系分散质微粒大小将分散系分为溶液、胶体和浊液,故③错误;
④根据水溶液或熔融态是否能够导电将化合物分为电解质和非电解质,故④错误;
故选D.
点评 本题考查物质的分类,题目难度不大,注意物质的分类的依据,不同的分类标准会得出不同的分类结果.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
11.下列说法中正确的是( )
| A. | 同周期金属元素,原子失电子能力越强,最高化合价越高 | |
| B. | 同主族的单核阴离子,其还原性越强,水解程度越大 | |
| C. | IA和VIIA族元素间可形成共价化合物 | |
| D. | 第二周期元素从左到右最高化合价从+1到+7 |
20.相同温度下,已知下面三个数据:①7.2×10-4、②2.6×10-4、③4.9×10-10分别是三种酸的电离平衡常数,若已知这三种酸可发生如下反应:NaCN+HNO2═HCN+NaNO2 NaNO2+HF═HCN+NaF NaNO2+HF═HNO2+NaF由此可判断下列叙述中正确的是( )
| A. | HF的电离常数是① | B. | HNO2的电离常数是① | ||
| C. | HCN的电离常数是② | D. | HNO2的电离常数是③ |
 节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染.实验小组同学欲测定空气中SO2的含量,并探究SO2的性质.
节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染.实验小组同学欲测定空气中SO2的含量,并探究SO2的性质.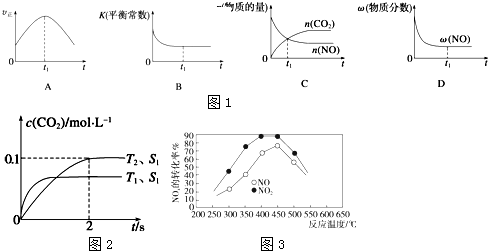
 .
. 在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分,当左边充入1molN2,右边充入8gCO和CO2的混合气体,隔板处于如图所示位置(两侧温度相同),则混合气体中CO和CO2的总物质的量为0.25mol,其中CO和CO2的分子数之比为3:1.
在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分,当左边充入1molN2,右边充入8gCO和CO2的混合气体,隔板处于如图所示位置(两侧温度相同),则混合气体中CO和CO2的总物质的量为0.25mol,其中CO和CO2的分子数之比为3:1.