题目内容
13.下列化学用语表示正确的是( )| A. | 氧的原子结构示意图: | B. | 甲烷的比例模型: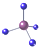 | ||
| C. | 硫化钾的电子式: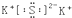 | D. | CO2的结构式:O-C-O |
分析 A.氧原子核外电子数为8,有2个电子层,各层电子数为2、6;
B.根据甲烷的比例模型与球棍模型的表示方法判断;
C.硫化钾为离子化合物,硫离子为阴离子,需要中括号且标明所带电荷数;
D.二氧化碳中C分别与2个O形成2对共价键,据此解答即可.
解答 解:A.氧原子核外电子数为8,有2个电子层,各层电子数为2、8,原子结构示意图为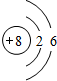 ,选项中为圆圈内无“+”号,故A错误;
,选项中为圆圈内无“+”号,故A错误;
B.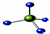 为甲烷的球棍模型,甲烷的比例模型为:
为甲烷的球棍模型,甲烷的比例模型为: ,故B错误;
,故B错误;
C.K2S为离子化合物,只含有离子键,电子式为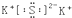 ,故C正确;
,故C正确;
D.二氧化碳中C与O形成两对共价键,结构简式为:O=C=O,故D错误,故选C.
点评 本题考查常用化学用语的书写判断,题目难度中等,注意掌握电子式、球棍模型与比例模型及元素符号的概念及正确表示方法,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
3.下列叙述正确的是( )
| A. | 在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应吸热 | |
| B. | 同温同压下,4Al(s)+3O2(g)═2Al2O3(s)在常温和点燃条件下的△H不同 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l);△H=-53.7KJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量大于53.7kJ | |
| D. | 需要加热的化学反应一定是吸热反应 |
4.在一定的温度下,向CH3COONa的稀溶液里加水稀释,下列各种量变小的是( )
①H+的物质的量浓度
②OH-的物质的量浓度
③c(CH3COO-)/c(CH3COOH)
④c(H+)•c(OH-)
①H+的物质的量浓度
②OH-的物质的量浓度
③c(CH3COO-)/c(CH3COOH)
④c(H+)•c(OH-)
| A. | ①② | B. | ② | C. | ②③ | D. | ②③④ |
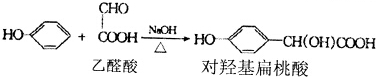
1.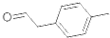 是对甲基苯乙醛的键线式,由它转化为对甲基苯乙炔(
是对甲基苯乙醛的键线式,由它转化为对甲基苯乙炔(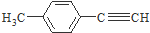 )的一条路线如下:
)的一条路线如下:
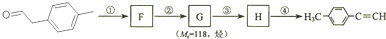
(1)对甲基苯乙醛的分子式为:C9H10O;
(2)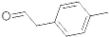 分子中一定在同一平面的原子数为12个;
分子中一定在同一平面的原子数为12个;
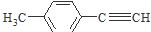 分子中在同一直线上的原子数最多有6个;
分子中在同一直线上的原子数最多有6个;
(3)写出①--④步反应所加试剂、反应条件和①--③步反应类型:
 是对甲基苯乙醛的键线式,由它转化为对甲基苯乙炔(
是对甲基苯乙醛的键线式,由它转化为对甲基苯乙炔( )的一条路线如下:
)的一条路线如下:
(1)对甲基苯乙醛的分子式为:C9H10O;
(2)
 分子中一定在同一平面的原子数为12个;
分子中一定在同一平面的原子数为12个; 分子中在同一直线上的原子数最多有6个;
分子中在同一直线上的原子数最多有6个;(3)写出①--④步反应所加试剂、反应条件和①--③步反应类型:
| 序号 | 所加试剂及反应条件 | 反应类型 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
18.下列各组物质的晶体中,晶体类型相同,化学键类型也完全相同的是( )
| A. | CO2和SiO2 | B. | CCl4和Fe | C. | CaCl2和HCl | D. | SO3和SO2 |
5.图是元素周期表的一部分,试用化学符号回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的是Ar(填具体元素符号),其原子结构示意图为 .
.
(2)在这些元素中,③的气态氢化物与⑧的气态氢化物反应的现象为冒白烟,产物的晶体类型为离子晶体.
(3)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物的电子式为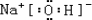 .
.
(4)⑥的单质与②、④形成的某种化合物反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(5)在⑦、⑧两种元素中,非金属性较强的是Cl(填具体元素符号),能证明这一结论的化学方程式为Cl2+H2S=2HCl+S.
(6)科学家借助元素周期表研究合成有特定性质的新物质,如在金属与非金属交界处寻找半导体材料.
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VIIA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 .
.(2)在这些元素中,③的气态氢化物与⑧的气态氢化物反应的现象为冒白烟,产物的晶体类型为离子晶体.
(3)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物的电子式为
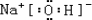 .
.(4)⑥的单质与②、④形成的某种化合物反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(5)在⑦、⑧两种元素中,非金属性较强的是Cl(填具体元素符号),能证明这一结论的化学方程式为Cl2+H2S=2HCl+S.
(6)科学家借助元素周期表研究合成有特定性质的新物质,如在金属与非金属交界处寻找半导体材料.
 .
.
 .
. .
. .
.