题目内容
【题目】某化学小组以环己醇![]() 制备环己烯。已知:
制备环己烯。已知:
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
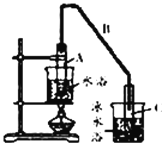
①写出环己醇制备环己烯的化学反应方程式:_________。
②A中碎瓷片的作用是_____________,导管B除了导气外还具有的作用是_____________。
③试管C置于冰水浴中的目的是_______________________。
(2)环己烯粗品中含有环己醇和少量酸性杂质等,需要提纯。
①加入饱和食盐水,振荡、静置、分层,水在______层(填上或下);分液后用_________(填入编号)洗涤。
a.KMnO4溶液 b.稀 H2SO4 c.Na2CO3溶液
②再将环己烯热馏,蒸馏时要加入生石灰,目的是__________。
③收集产品时,控制的温度应在_________左右。
(3)以下区分环己烯精品和粗品的方法,合理的是_______。
a.用酸性高锰酸钾溶液 b.用金属钠 c.溴水
【答案】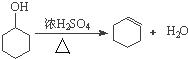 防止暴沸 冷凝 防止环己烯挥发 下 c 除去环己烯中混有的少量水 83℃ b
防止暴沸 冷凝 防止环己烯挥发 下 c 除去环己烯中混有的少量水 83℃ b
【解析】
(1)①环己醇在浓硫酸的作用下分子内脱水生成环己烯,反应为: ,因此,本题正确答案是:
,因此,本题正确答案是: 。
。
②发生装置A中碎瓷片的作用是防止暴沸,因为生成的环己烯的沸点为83℃,要得到液态环己烯,导管B除了导气外还具有冷凝作用,便于环己烯冷凝.因此答案是:防止暴沸;冷凝。
③冰水浴的目的是降低环己烯蒸气的温度,使其液化,因此答案是:进一步冷却,防止环己烯挥发。
(2)①环己烯是烃类,不溶于氯化钠溶液,密度0.81g/cm3,密度比水小,振荡、静置、分层后环己烯在上层,水在下层;因为分液后环己烯粗品中还含有少量的酸和环己醇,不能用酸,也不能用酸性高锰酸钾,否则会氧化环己烯,可用Na2CO3溶液洗涤除去酸,因此答案是:下;c;
②生石灰能与水反应生成氢氧化钙,除去了残留的水,得到纯净的环己烯,因此答案是:除去环己烯中混有的少量水。
③根据表中数据可以知道,馏分环己烯的沸点为83℃,故收集产品应控制温度在83℃左右;答案:83℃。
(3)区别粗品与精品可加入金属钠,观察是否有气体产生,若无气体,则是精品,酸性高锰酸钾溶液和溴水均能与环己烯反应,因此,本题正确答案是:b。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案