题目内容
【题目】将64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为22.4 L。请计算(写出计算过程):
(1)NO标况下的体积________
(2)参加反应的HNO3的物质的量________。
【答案】设NO标况下的物质的量为xmol,NO2标况下的物质的量为ymol
x+y=![]()
3x+y=![]() ×2
×2
解得:x=0.5,y=0.5
NO在标况下的体积为0.5×22.4=11.2L 参加反应的HNO3的物质的量为![]() ×2+
×2+![]() =3mol
=3mol
【解析】
本题考查氧化还原反应的计算,物质的量浓度的计算,可根据电子得失守恒及元素守恒列方程式解即可。
(1)64g的物质的量![]() ,在反应中失去电子的物质的量是
,在反应中失去电子的物质的量是![]() ,22.4L混合气体的物质的量
,22.4L混合气体的物质的量![]() ,设NO标况下的物质的量为xmol,NO2标况下的物质的量为ymol
,设NO标况下的物质的量为xmol,NO2标况下的物质的量为ymol
元素守恒:x+y=![]()
电子得失守恒:3x+y=![]() ×2
×2
解得:x=0.5,y=0.5
NO在标况下的体积为0.5mol×22.4L/mol=11.2L。故正确答案为:
解:设NO标况下的物质的量为x mol,NO2标况下的物质的量为y mol
x+y=![]()
3x+y=![]() ×2
×2
解得:x=0.5,y=0.5
NO在标况下的体积为0.5mol×22.4L/mol=11.2L。
(2)参加反应的硝酸的物质的量是酸性的硝酸根和氧化性的硝酸的物质的量之和,即![]() ×2+
×2+![]() =3mol,故正确答案为:参加反应的HNO3的物质的量为
=3mol,故正确答案为:参加反应的HNO3的物质的量为![]() ×2+
×2+![]() =3mol。
=3mol。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某化学小组以环己醇![]() 制备环己烯。已知:
制备环己烯。已知:
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
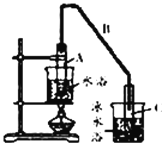
①写出环己醇制备环己烯的化学反应方程式:_________。
②A中碎瓷片的作用是_____________,导管B除了导气外还具有的作用是_____________。
③试管C置于冰水浴中的目的是_______________________。
(2)环己烯粗品中含有环己醇和少量酸性杂质等,需要提纯。
①加入饱和食盐水,振荡、静置、分层,水在______层(填上或下);分液后用_________(填入编号)洗涤。
a.KMnO4溶液 b.稀 H2SO4 c.Na2CO3溶液
②再将环己烯热馏,蒸馏时要加入生石灰,目的是__________。
③收集产品时,控制的温度应在_________左右。
(3)以下区分环己烯精品和粗品的方法,合理的是_______。
a.用酸性高锰酸钾溶液 b.用金属钠 c.溴水
【题目】一定温度下,10 mL 0.40 mol·L-1 H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.反应到6 min时,c(H2O2)=0.30 mol·L-1
B.0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol·L-1·min-1
C.6~10 min的平均反应速率:v(H2O2)<3.3×10-2 mol·L-1·min-1
D.反应到6 min时, H2O2分解了50%
【题目】Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用相应的化学用语答题)
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(1)R的元素符号为________;M在元素周期表中的位置为________________。
(2)X与Y按原子个数比1∶1构成的物质的电子式为________________;所含化学键类型__________________________。
(3)X+、Y2-、M2-离子半径大小顺序为__________________。
(4)将YM2通入FeCl3溶液中的离子方程式:_________________________________________。
Ⅱ.如图转化关系(A、B、C中含相同元素)
![]()
![]()
![]()
![]()
![]()
(1)若B为白色胶状不溶物,则A与C反应的离子方程式为_________________________。
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应生成B的离子方程式为_____________________________________________。
【题目】下列离子方程式正确且与对应操作和目的相符的是
选项 | 目的 | 操作 | 离子方程式 |
A | 比较Fe2+和Br还原性强弱 | 向FeBr2溶液中滴入少量氯水 | 2Br+Cl2=Br2+2Cl |
B | 比较C、Si非金属性强弱 | 向硅酸钠溶液中通入少量二氧化碳 | SiO32-+CO2+H2O=H2SiO3↓+CO32- |
C | 除去CO2中的SO2 | 将气体通入盛有饱和碳酸氢钠溶液的洗气瓶 | CO32-+SO2= SO32-+CO2 |
D | 实验室制取氯气 | 向MnO2固体中加入浓盐酸并加热 | MnO2+4HCl(浓) +2Cl +Cl2↑+2H2O |
A.AB.BC.CD.D