题目内容
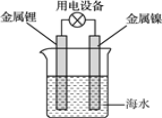
【题目】如图所示为科学家正在研发的新型电池,该电池容量大,电流稳定等多方面优点。该电池的电池总反应式为:Na(1-x)MO2+NaxCn![]() NaMO2+nC,下列说法正确的是( )
NaMO2+nC,下列说法正确的是( )

A.电池充电时,NaMO2电极为阳极
B.放电时,负极反应式:NaMO2-xe-=Na(1-x)MO2+xNa+
C.电解质可以选用无水乙醇
D.充电时,阳极反应式为:nC+xNa++xe-=NaxCn
【答案】B
【解析】
A、充电时,钠离子移向左侧,左侧电极为阴极;
B、原电池中,负极发生失电子的氧化反应;
C、无水乙醇为非电解质;
D、电解池中,阳极上发生失电子的氧化反应。
A、充电时,钠离子移向左侧,NaMO2电极为阴极,故A错误;
B、原电池中,负极发生失电子的氧化反应:放电时,负极电极反应时为:NaMO2-xe-=Na(1-x)MO2+xNa+,故B正确;
C、无水乙醇为非电解质,不能电离,不导电,故C错误;
D、电解池中,阳极上发生失电子的氧化反应:电极反应式为NaxCn-xe-═nC+xNa+,故D错误。
答案选B。

练习册系列答案
相关题目