题目内容
已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈—1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
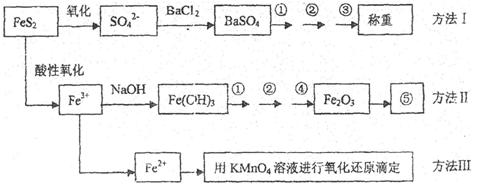
请同答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________、②___________、③________。
操作④、⑤用到的主要仪器是:④_________、⑤__________(每空填1~2个仪器)。
(2)判断溶液中SO42-离子己沉淀完全的方法是______________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________。

请同答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________、②___________、③________。
操作④、⑤用到的主要仪器是:④_________、⑤__________(每空填1~2个仪器)。
(2)判断溶液中SO42-离子己沉淀完全的方法是______________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
| A.砝码生锈 | B.定容时俯视 |
| C.称量时物质和砝码位置反了(需要游码) | D.容量瓶用待装液润 |
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________。
(15分)(1)过滤(1分) 洗涤(1分) 干燥(1分) 坩埚、酒精灯(1分) 天平(1分)
(2)取上层清液滴加BaCl2溶液,若无白色沉淀生成,说明SO42-沉淀完全(2分)
(3)A、B、D (3分)
(4)有三个可能的原因:
①Fe(OH)3沉淀表面积大,易吸附杂质 (1分)
②过滤洗涤时未充分将吸附的杂质洗去 (1分)
③Fe(OH)3灼烧不充分,未完全转化为Fe2O3 (1分)u
(5)75.0%(2分)。
(2)取上层清液滴加BaCl2溶液,若无白色沉淀生成,说明SO42-沉淀完全(2分)
(3)A、B、D (3分)
(4)有三个可能的原因:
①Fe(OH)3沉淀表面积大,易吸附杂质 (1分)
②过滤洗涤时未充分将吸附的杂质洗去 (1分)
③Fe(OH)3灼烧不充分,未完全转化为Fe2O3 (1分)u
(5)75.0%(2分)。
略

练习册系列答案
相关题目
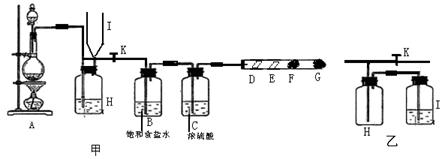
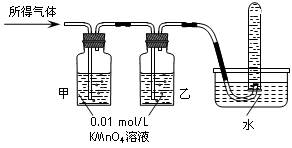
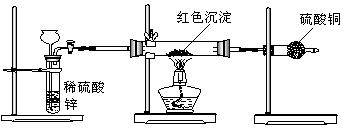
 CuSO4+SO2↑+2H2O,如图是铜与浓硫酸反应的实验装置图,请回答下列问题。
CuSO4+SO2↑+2H2O,如图是铜与浓硫酸反应的实验装置图,请回答下列问题。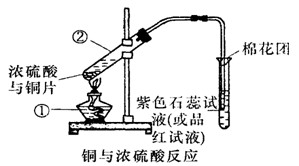
 在一支洁净的试管内混合后,向其中又加入0.5mL乙醛溶液,然后水浴加热,结果无红色
在一支洁净的试管内混合后,向其中又加入0.5mL乙醛溶液,然后水浴加热,结果无红色 的气体直接通入苯酚钠溶液中,看是否有浑浊出现
的气体直接通入苯酚钠溶液中,看是否有浑浊出现