题目内容
【题目】在2L的密闭容器中放入4molN2O5,发生如下反应:2N2O5(g)![]() 4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,求:
4NO2(g)+ O2(g)。反应5min后,测得N2O5转化了20%,求:
(1)υ(NO2)、υ(O2)分别为多少?
(2)5min时,N2O5占混合气体总体积的百分比是多少?
(要求写出计算过程)
【答案】(1)υ(NO2)=0.16mol/(L·min)υ(O2)=0.O4mol/(L·min)(2)61.5%
【解析】
试题 2N2O5(g)![]() 4NO2(g)+ O2(g)
4NO2(g)+ O2(g)
起始浓度(mol/L) 2 0 0
转化浓度(mol/L) 2×0.2 0.8 0.2
5min后浓度(mol/L) 1.6 0.8 0.2
所以5分钟内υ(NO2)=0.8mol/L÷5min=0.16mol/(L·min)
υ(O2)=0.2mol/L÷5min=0.04mol/(L·min)
5min时,N2O5占混合气体总体积的百分比是![]()

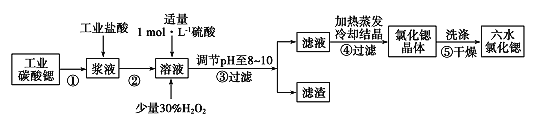
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 |
HClO | 3×10-8 |
H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
H2C2O4 | K1=5.4×10-2 K2=5.4×10-5 |
H2S | K1=1.3×10-7 K2=7.1×10-15 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是____。
(2)常温下0.1 mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母)。
A.c(H+) B.![]() C.
C.![]() D.c(OH-)
D.c(OH-)
(3)0.1 mol/L的H2C2O4溶液与0.1mol/L的KOH的溶液等体积混合后所得溶液中各离子浓度由大到小的顺序为__________________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COOK________NaClO (填“>”、“<”或“=”)。
(5)向0.1mol/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=______________。
(6)向NaClO溶液中通入少量的CO2,所发生的离子方程式为___________。