��Ŀ����
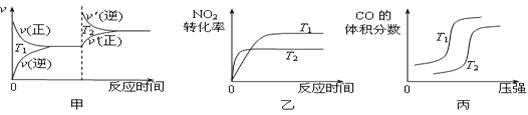
����Ŀ��ij�¶�ʱ����ӦX(g)![]() 4Y(g)��Z(g) ��H����Q kJ��mol��1��2 L�����ܱ������н��У�X��Z��Ũ����ʱ��仯��ͼ��ʾ������˵������ȷ����
4Y(g)��Z(g) ��H����Q kJ��mol��1��2 L�����ܱ������н��У�X��Z��Ũ����ʱ��仯��ͼ��ʾ������˵������ȷ����

A. 2 min�ڣ�X��ƽ����Ӧ����Ϊ0.25 mol��L��1��min��1
B. ��t minʱ���÷�Ӧ�ﵽƽ��״̬
C. ��5 min��X������������Z��������������ұ��ֲ���
D. 5 min�ڣ���Ӧ�ų�������Ϊ1.6Q kJ
���𰸡�B
��������
A. 2 min�ڣ�VX=C/t=0.5/2=0.25 mol��L��1��min��1,����ȷ��
B. ��t minʱ��X�����ʵ�����Ũ���ټ��٣�Z��Ũ�������ӣ���Ӧ������У�δ�ﵽƽ��״̬���ʴ���
C. ��5 min��X��Z��Ũ�Ⱥ���ϲ��ڸı䣬����ƽ��״̬��X��Z��ϵ����ȣ���X������������Z��������������ұ��ֲ��䣬��ȷ��
D. 5 min�ڣ�����X�����ʵ�����(0.9-0.1)*2=1.6 mol���ų���������1.6Q kJ������ȷ��˵������ȷ����B��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��һ�������£����и���������һ��ʵ��ͼ����ʾת����ϵ����

ѡ�� | X | Y | Z | W |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | Fe3O4 | Fe | FeCl2 | FeCl3 |
C | H2SO4 | SO2 | S | SO3 |
D | CH3CH2Br | CH2=CH2 | C2H5OH | CH2BrCH2Br |
A. A B. B C. C D. D