题目内容
【题目】煤的气化和液化是现代能源工业中重点考虑的综合利用技术。最常见的气化方法是用煤作原料生产水煤气,而比较流行的液化方法是煤在催化剂等条件下生产CH3OH。
已知制备甲醇的有关化学反应如下:
①CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H1=-90.8 kJmol-1
②CO(g)+H2O(g)CO2(g)+H2(g)△H2=-412 kJmol-1
③CO(g)+2H2(g)CH3OH(g)△H3
I.回答下列问题:
(1)欲提高甲醇的产率,可以采取的措施有______(填字母序号)。
A.升高温度
B.增大压强
C.降低温度
D.降低压强
(2)提高甲醇反应选择性的关键因素是______。
(3)保持温度和容积不变,下列描述能说明反应③达到平衡状态的是______(填字母序号)。
A.v(CO):v(H2):v(CH3OH)=1:2:1
B.混合气体的压强不再随时间的变化而变化
C.单位时间内断裂2 mol H-H键,同时生成3mol C-H键
D.一段时间内的平均反应速率等于0
E.混合气体的平均摩尔质量保持不变
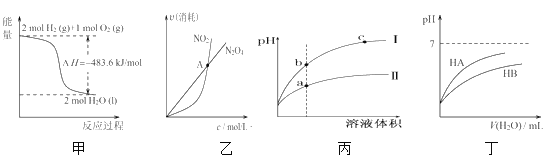
Ⅱ.在一密闭容器中投入1mol CO和2molH2发生反应③,实验测得平衡时甲醇的物质的量随温度、压强变化关系如图1所示:
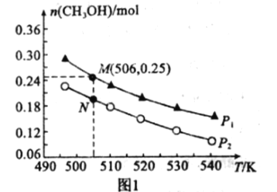
(1)压强P1______P2(填“>”、“<“或”=”)。
(2)M、N两点的化学反应速率:vM______vN(填“>”、“<“或“=”)
(3)对于气相反应,用某组分B的平衡压强P(B)代替物质的量浓度c(B)也可表示平衡常数(Kp),则M点时,平衡常数Kp=______(P1=5 MPa)。
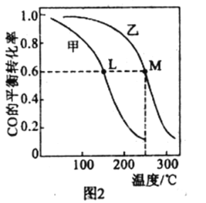
(4)甲、乙两个恒容密闭容器的体积相同,向甲中加入 1molCO和 2mol H2,向乙中加入2mol CO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)______2P(L),平衡常数:K(M)______K(L)(填“>”、“>”或“=”)。
【答案】BC 合适的催化剂 BDE > > ![]() > <
> <
【解析】
I.(1)首先根据盖斯定律,写出CO(g)+2H2(g)=CH3OH(g)的热化学反应方程式,然后根据勒夏特列原理进行分析;
(2)提高甲醇反应选择性的关键因素是合适的催化剂;
(3)根据化学平衡状态的定义进行分析;
II.(1)作等温线,增大压强,平衡向正反应方向进行,CH3OH的物质的量增大,据此分析;
(2)利用压强对反应速率的影响进行分析;
(3)利用“三段式”法进行计算;
(4)平衡常数只受温度的影响,正反应为放热反应,温度越高,化学平衡常数越小;
I.(1)根据目标反应方程式,以及盖斯定律,①+②得出△H3=(-90.8kJ·mol-1-412kJ·mol-1)=-502.8kJ·mol-1,
A.该反应为放热反应,升高温度,平衡向逆反应方向进行,甲醇的产率降低,故A不符合题意;
B.根据反应方程式,增大压强,平衡向正反应方向进行,甲醇物质的量增大,即产率增大,故B符合题意;
C.该反应为放热反应,降低温度,平衡向正反应方向进行,甲醇物质的量增大,即产率增大,故C符合题意;
D.降低压强,平衡向逆反应方向进行,甲醇物质的量减少,产率降低,故D不符合题意;
故答案选BC;
(2)提高甲醇反应选择性的关键因素是选择合适的催化剂;
(3) A.没有指明反应的方向,因此无法判断是否达到平衡,故A不符合题意;
B.恒温恒容下,反应前后气体系数之和不相等,因此当压强不再改变,说明反应达到平衡,故B符合题意;
C.断裂H-H键和生成C-H键,反应都是向正反应方向进行,因此单位时间内断裂2molH-H键,同时生成3molC-H键,不能说明反应达到平衡,故C不符合题意;
D.当达到平衡时,同种物质消耗量和生成量相等,即一段时间内的平均反应速率等于0,故D符合题意;
E.根据![]() ,组分都是气体,所以气体质量不变,反应前后气体系数之和不相等,因此当平均摩尔质量不变时,说明反应达到平衡,故E符合题意;
,组分都是气体,所以气体质量不变,反应前后气体系数之和不相等,因此当平均摩尔质量不变时,说明反应达到平衡,故E符合题意;
故答案选BDE;
II.(1)根据反应方程式,增大压强,平衡向正反应方向移动,CH3OH物质的量增多,根据图像,作等温线,P1对应甲醇的物质的量大于P2时的,因此P1>P2;
(2)M、N两点温度相等,M点的压强大于N点压强,压强越大,反应速率越快,v(M)>v(N);
(3)利用“三段式”进行分析,M点CH3OH物质的量为0.25mol,因此有 平衡常数Kp=
平衡常数Kp=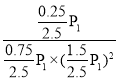 =
=![]() ;
;
(4)M点和L点,CO的转化率相同,因为体积相同,且乙中气体是甲中气体的2倍,则相同温度是P(M)=2P(L),M点温度高,因此P(M)>2P(L);平衡常数只与温度有关,该反应为放热反应,温度越高反应进行的限度越小,平衡常数越小,因此K(M)<K(L)。

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案