��Ŀ����
����Ŀ���飨83��Ԫ�أ���Ҫ��������Ͻ���Ͻ��������ʱ�����������ԣ���������ӡˢǦ�ֺ߾������͡�ʪ�������¹�����������������Ҫ�ɷ�Ϊ![]() ������
������![]() ��
��![]() ��
��![]() ���ʣ�Ϊԭ����Bi�Ĺ����������£�
���ʣ�Ϊԭ����Bi�Ĺ����������£�
��֪����.![]() ������ˮ��������700���ͷֽ�����
������ˮ��������700���ͷֽ�����![]() ��
��![]() �ķе�Ϊ447����
�ķе�Ϊ447����
��.25��ʱ��![]() ��
��![]() ��
��
�ش��������⣺
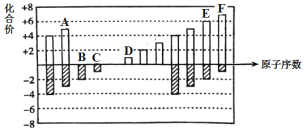
��1������Ԫ�����ڱ��е�λ��Ϊ___________________��
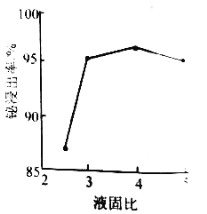
��2����������ʱ��������Ũ��![]() �������¶�70��������ʱ��2h����ͬ����Һ�̱������½��н���ʵ�飬��������Һ�̱ȵĹ�ϵ��ͼ��ʾ������ʵ�Һ�̱�Ӧѡ__________��
�������¶�70��������ʱ��2h����ͬ����Һ�̱������½��н���ʵ�飬��������Һ�̱ȵĹ�ϵ��ͼ��ʾ������ʵ�Һ�̱�Ӧѡ__________��
��3�����������ijɷ�Ϊ_____________���ѧʽ����
��4�����������Ļ�ѧ����ʽΪ___________________��
��5������ͭ��ʱ��������Һ���м���NaOH��Һ����pH���ٽ�![]() ˮ������
ˮ������![]() ����˹�����
����˹�����![]() ˮ������ӷ���ʽΪ_________________________��������Һ����
ˮ������ӷ���ʽΪ_________________________��������Һ����![]() Ϊ
Ϊ![]() ��������������NaOH��Һʱ��pHǡ��Ϊ6�����ֳ���
��������������NaOH��Һʱ��pHǡ��Ϊ6�����ֳ���![]() ����ʱ
����ʱ![]() ��ȥ����Ϊ________��������Һ����仯����
��ȥ����Ϊ________��������Һ����仯����
��6������Һ��������Ũ����ɷ���____________����ѭ��ʹ�á�
���𰸡��������ڵ�VA�� 3 ![]() ��
��![]()
![]()
![]() 97.6% ����
97.6% ����
��������
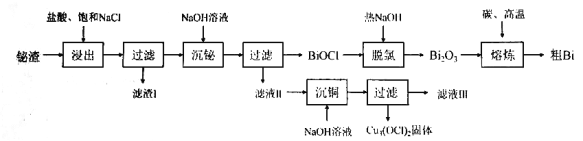
���ݹ�������ͼ������֪�������м�������ͱ��͵�NaCl��Һ�����˺�õ�AgCl��PbCl2������������Һ�м���NaOH��Һ�����˵õ�BiOCl�ij�������Һ����BiOCl���ȵ�NaOH���ȵõ�Bi2O3��Bi2O3�ڸ��������±�̼��ԭ�õ���Bi������Һ���м���NaOH��Һ����pH���ٽ�Cu2+ˮ������Cu3(OCl)2��NaCl��Һ���ݴ˷���������⡣
(1)��Ԫ���뵪Ԫ��ͬ���壬��Ԫ�����ڱ��е�λ���ǵ������ڵ���A�壬�ʴ�Ϊ���������ڵ�VA�壻
(2)��ͼ���֪��Һ�̱�Ϊ3��4ʱ��Ľ����ʽϸߣ��Խ�Լԭ��Ϊԭ��Һ�̱�Ϊ3ʱ��Ϊ���ʣ��ʴ�Ϊ��3��
(3)��������������֪���������ijɷ���AgCl��PbCl2���ʴ�Ϊ��AgCl��PbCl2��
(4)��������ʱ��BiOCl���ȵ�NaOH��Ӧ�õ�Bi2O3��NaCl����Ӧ����ʽΪ2BiOCl+2NaOH![]() Bi2O3+2NaCl+H2O���ʴ�Ϊ��2BiOCl+2NaOH
Bi2O3+2NaCl+H2O���ʴ�Ϊ��2BiOCl+2NaOH![]() Bi2O3+2NaCl+H2O��
Bi2O3+2NaCl+H2O��
(5)����ͭ��ʱ������Һ���м���NaOH��Һ����pH���ٽ�Cu2+ˮ������Cu3(OCl)2����Ӧ�����ӷ���ʽΪ��3Cu2++2H2O+2Cl-===Cu3(OCl)2��+4H+������������NaOH��Һʱ��pH=6����Һ��c(H+)=10-6mol��L-1����c(OH-)=10-8mol��L-1������Ksp[Cu(OH)2]=c(Cu2+)��c2(OH-)����c(Cu2+)=0.00012mol/L��n(Cu2+)=0.00012mol/L��2VL=0.00024Vmol����ȥ����Cu2+�����ʵ���Ϊ0.01Vmol-0.00024Vmol=0.00976V mol��Cu2+��ȥ����Ϊ![]() ���ʴ�Ϊ��3Cu2++2H2O+2Cl-===Cu3(OCl)2��+4H+��97.6%��
���ʴ�Ϊ��3Cu2++2H2O+2Cl-===Cu3(OCl)2��+4H+��97.6%��
(6)��Һ��ΪNaCl��Һ��������Ũ����ɷ��ؽ�������ѭ��ʹ�ã��ʴ�Ϊ��������