题目内容
10.分子的性质是由分子的结构决定的,通过对下列分子结构的观察来推测它的性质:
(1)此有机物中含有的官能团氯原子、碳碳双键(填名称)
(2)苯基部分可发生加成反应和氧化反应(填反应类型).
(3)-CH═CH2部分可发生加成反应和加聚反应等,检验此官能团所用试剂为溴水
(4)写出此有机物形成的高分子化合物的结构简式:
 .
.(5)试判断此有机物的-C(CH2Cl)3部分不能(填“能”或“不能”)发生消去反应.
分析 由结构简式可知,苯基部分有氢原子,可发生取代反应,同时苯基是不饱和的,可以发生加成反应;而-CH═CH2可以发生加成反应和氧化反应;-C(CH2Cl)3部分中心碳原子上没有氢原子,所以不能发生消去反应,以此解答该题.
解答 解:(1)有机物的结构简式可以得到含有的官能团为氯原子和碳碳双键,故答案为:氯原子、碳碳双键;
(2)分子中含有碳碳双键,可发生加成、加聚和氧化反应,故答案为:加成;氧化;
(3)碳碳双键可以和溴水之间反应使溴水褪色,可以据此检验双键的存在,此外碳碳双键还可以发生加聚反应,故答案为:加成;加聚;溴水;
(4)分子中含有碳碳双键,可发生加聚反应,生成物为 ,故答案为:
,故答案为: ;
;
(5)-C(CH2Cl)3部分中心碳原子上没有氢原子,所以不能发生消去反应,故答案为:不能.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系解答的关键,侧重烯烃、卤代烃性质的考查,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
16.在下列溶液中,能大量共存的离子组是( )
| A. | 能使pH试纸显蓝色的溶液中:K+、Ba2+、H+、Br- | |
| B. | 加入Al能放出H2的溶液中:K+、Na+、NO3-、Cl- | |
| C. | 含有大量Fe3+的溶液中:SCN-、I-、K+、Br- | |
| D. | 能使石蕊试液显红色的溶液中:K+、SO42-、S2-、CO32- |
1.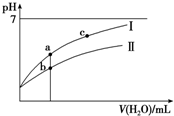 已知:25°C时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
已知:25°C时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
 已知:25°C时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
已知:25°C时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 图象中a、c两点处的溶液中$\frac{c({R}^{-})}{c(O{H}^{-})•c(HR)}$相等(HR代表CH3COOH或HClO) | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
18.下列化学用语中正确的是( )
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: | B. | NH4Cl的电子式: | ||
| C. | 含78个中子的碘的核素:53131I | D. | 二氧化硅的分子式:SiO2 |
5.下列有关化学反应表达正确的是( )
| A. | 服用阿司匹林过量出现水杨酸(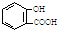 )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: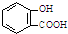 +2HCO3-→ +2HCO3-→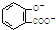 +2 CO2↑+2 H2O +2 CO2↑+2 H2O | |
| B. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O | |
| C. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- |
15.下列说法中,正确的是( )
| A. | 苯酚和苯都能和溴水发生苯环上的取代反应 | |
| B. | 醇属于烃的衍生物,饱和一元醇的组成符合CnH2nO | |
| C. | 乙醇是无色透明的液体,密度比水小,能用乙醇从碘水中萃取出碘 | |
| D. | 向苯酚钠溶液中通入CO2气体,使溶液变浑浊,说明碳酸的酸性比苯酚的强 |
2.向硝酸钠溶液中加入铜粉不发生反应,若再加入某种盐,则铜粉可以逐渐溶解,符合此条件的盐是( )
| A. | ZnSO4 | B. | NaHCO3 | C. | NaHSO4 | D. | Fe(NO3)2 |
19.下列各组气体通常条件下能稳定共存( )
| A. | NH3 O2 HCl | B. | H2S O2 SO2 | C. | CO2 HI Cl2 | D. | N2 H2 HCl |
 ;
; 或
或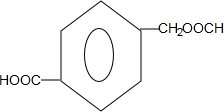 ;
;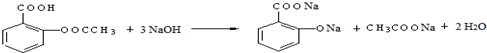 ;
;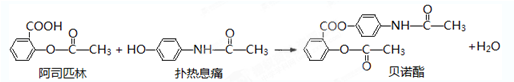 .
.