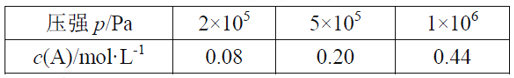题目内容
【题目】在2 L恒容密闭容器中充入![]() 、
、![]() ,在一定条件下发生如下反应:
,在一定条件下发生如下反应:![]()
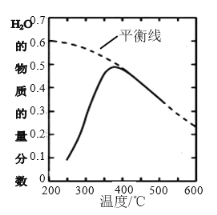
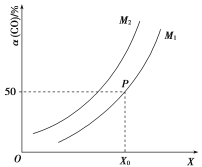
![]() ;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
A.工业上,利用上述反应合成甲醇,温度越高越好
B.图象中X代表温度,![]()
C.图象中P点代表的平衡常数K为![]()
D.温度和容积不变,再充入![]() 、1 mol CO,达到平衡时CO的转化率减小
、1 mol CO,达到平衡时CO的转化率减小
【答案】C
【解析】
A.该反应的正反应是放热反应,温度升高,平衡向左移动,甲醇的产率降低,应根据催化剂来选择合适的温度,A项错误;
B.该反应的正反应是放热反应,又是气体分子数减小的反应,从图象看出,随着X增大,CO的转化率增大,所以X代表压强,M代表温度,温度越高,CO的平衡转化率越低,所以![]() ,B项错误;
,B项错误;
C.P点时CO的转化率为50%,用“三段式”法进行计算:
![]()
起始浓度/(![]() ) 1 0.5 0
) 1 0.5 0
变化浓度/(![]() ) 0.5 0.25 0.25
) 0.5 0.25 0.25
平衡浓度/(![]() ) 0.5 0.25 0.25
) 0.5 0.25 0.25
![]() (单位可省),C项正确;
(单位可省),C项正确;
D.温度不变,平衡常数不变,容积不变,再充入![]() 、1 mol CO,相当于增大压强,平衡向右移动,
、1 mol CO,相当于增大压强,平衡向右移动,![]() 、CO的转化率都增大,D项错误。
、CO的转化率都增大,D项错误。
答案选C。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目